静脉注入的放射性胶体颗粒约85%被库普弗细胞吞噬,从而使肝实质显影;其余15%则被脾和骨髓等的巨噬细胞摄取。根据肝内显像剂的分布状况,可以判断肝的位置、大小、形态以及有无占位性病变,从而达到诊断疾病的目的。2)99m Tc-植酸钠植酸钠本身不是胶体颗粒,而当它经静脉注入体内后,与血中钙离子螯合形成不溶性的99m Tc-植酸钙胶体,可以被肝的库普弗细胞吞噬而显像。......
2023-12-07
9.8 肝肿瘤阳性显像
【原理】 利用肝肿瘤细胞选择性摄取某些放射性显像药物,直接把肿瘤的部位、大小、数量和形态显示出来而肝不显像的方法,称为肝癌阳性显像。放射性核素肝肿瘤阳性显像,以放射性浓聚区(“热区”)显示肝肿瘤病灶,是放射性核素肝肿瘤显像技术的一大进步。利用与肝癌组织具有特殊亲和力的放射性核素、标记化合物或肿瘤特异抗体在肝癌组织中大量浓聚,可直接显示肝癌的部位、大小、数量和形态,对于肝癌的定性、定位诊断具有特殊意义。
【检查方法】
(1)显像剂
1)“亲”肝肿瘤放射性核素类 例如67 Ga、201 Tl、111In。其中67 Ga为应用最早和最广泛的一种亲肿瘤显像剂,88%的肝细胞癌有浓集67 Ga的能力而获阳性显像,约有10%的假阳性和少数假阴性(肝癌组织血供不良或有出血坏死)。67 Ga的不足之处是炎症病灶(特别是化脓性炎症)亦可浓集此显像剂,这是产生假阳性结果的主要原因。67Ga显像的机制尚不十分明确,有如下学说:67Ga属于元素周期表中ⅢA族,它的生物特性与三价铁离子相似,经静脉注射后至少可与4种含铁蛋白(即转铁蛋白、乳铁蛋白、含铁蛋白和含铁细胞)相结合,但主要与转铁蛋白结合成复合物,然后与肿瘤细胞表面特异性铁蛋白受体作用进入细胞内,Hoffer等则认为,乳铁蛋白在肿瘤细胞摄取67 Ga中起关键作用。某些肿瘤产生过量乳酸,使肿瘤细胞外的pH值降低,67Ga脱离转铁蛋白后与肿瘤细胞膜上的乳铁蛋白结合,通过离子载体作用进入细胞,沉积在细胞质内的溶酶体中。另一方面,在肝硬化基础上的弥漫性癌变呈阴性结果,又使其敏感性降低。
2)标记药物类 例如99mTc-葡庚酸盐(99mTc-GH)、99mTc-(V)-DMSA、99mTc-MIBI。
3)肝胆显像剂 例如99mTc-PMT或99mTc-EHIDA。肝细胞癌起源于肝细胞,因此有可能摄取放射性肝胆显像剂,但正常肝摄取显像剂后立即通过分泌、排泄的过程,将其排入胆管系统,使肝区放射性迅速降低。而肝癌病灶缺乏有效的胆管系统,摄入的放射性肝胆显像剂无法被及时排出,因此,放射性滞留于病灶部位,呈“热区”表现。通常需要在肠道排泄相后病灶方能显示,故要进行“延迟显像”。
4)放射免疫显像剂 例如131I、111In、90Y等标记的抗AFP抗体、抗铁蛋白抗体,其是通过与肝癌细胞表面抗原的特异性结合,从而使肝癌显像。
5)正电子放射性药物 例如13N-氨、18F-FDG等。
(2)检查方法 静脉注射放射性药物。在注入放射性药物的同时开启γ相机,作肝血流灌注动态采集,每秒1帧,共60s。早期影像:5min时采集肝正位、右侧位、后位影像,500~1000k计数。若需了解胆道功能,按胆系显影方法采集至60min。在注射显像剂后的1h、2h、5 h分别采集肝正位、右侧位、后位静态影像。必要时在延迟相加作全身扫描或断层显像。
【注意事项】
(1)为减少胆囊影的影响,检查前和检查过程中嘱患者进食。
(2)拍摄延迟相时尽可能将肠道排除在外,以显示肝影。(www.chuimin.cn)
(3)注意肝细胞癌与肝腺瘤、肝再生结节及肝内胆管扩张的鉴别诊断。
【影像分析及结果判断】肝实质显像,发现占位性病变后2~3 d,即可进行本项检查。常规采集前位、后位及右侧位影像,特别要注意对占位最清晰的体位进行显像,方便对比分析。
(1)67 Ga显像 67 Ga是回旋加速器生产的放射性核素,物理半衰期为78 h,电子俘获方式衰变,发射的主要γ射线是93(41%)keV、185(93%)keV、300(81%)keV和394(4%)keV。常用的标记化合物为67 Ga-柠檬酸盐,给药剂量为74~185 MBq(2~5 mCi)静脉注射给药。SPECT能谱置于185 keV;若采用多能装置则同时置93 keV、185 keV、300 keV,可增加计数率,窗宽为20%,采用低能或中能准直器,给药后24~96 h(以48~72 h显像最佳)置患者于探头下行正侧位平面显像和断层显像。显像结果与肝实质显像对照,如果原放射性缺损区被填充,则说明病变区亲和了恶性肿瘤显像剂,诊断为肝癌的可能性很大。诊断时应排除肝炎性病变、肝脓肿和继发性肝癌,若67 Ga显像仍为放射性缺损区,则恶性肿瘤可能性较小。
(2)99m Tc-PMT阳性显像 99m Tc-PMT为较理想的肝胆显像剂之一,其与胆汁一样可被肝实质细胞摄取分泌和排泄,也可被肝癌和肝腺瘤细胞摄取和分泌,但后者(即癌瘤细胞病灶)无胆管系统供其排泄,故99m Tc-PM T被其摄取分泌后,可在其中较长时间聚集,在注射显像剂2~5 h做延迟显像时,正常肝放射性已由胆管系统完全排出,而癌细胞病灶区仍滞留大量的放射性,形成“热区”显像。99mTc-PMT静脉注射量185~740MBq(5~20mCi)。检查前要进食,以减少胆囊浓聚放射性的干扰。静脉注射99mTc-PMT5min后,肿瘤部位呈现出放射性减低区(“冷区”),但2~5h延迟显像该放射性减低区变为放射性浓聚区(“热区”)。肝癌与肝组织的放射性比值可达4∶1,肝腺瘤与肝组织放射性的比值更高达10∶1。99mTc-PMT延迟显像对于肝细胞癌的诊断具有较高的特异性,优于目前较好的肿瘤阳性显像剂(如67 Ga-枸橼酸盐等)。它的临床价值为:①用于小肝癌的定位及定性诊断,所显示的最小肝癌直径为2cm;②对临床诊断较困难、占肝癌总数30%左右的AFP阴性肝癌的诊断有独特价值,99mTc-PMT延迟显像的阳性率达62.2%;③用于原发性与继发性肝癌的鉴别诊断,99mTc-PMT延迟显像阳性的肿瘤可排除继发性肝癌。另外,99mTc-PMT肝显像可直观地显示肝肿瘤的大小、数量和部位,为手术提供参考。其对肝癌肝外转移灶的寻找及肝腺瘤的诊断也有较大价值。
(3)放射免疫显像 利用免疫学原理,将放射性核素标记抗体引入体内,使其定向地与肿瘤相关抗原结合,用核仪器显示肿瘤的位置大小,称为放射免疫显像(radioimmunoimaging,RII)。可用于肿瘤原发灶的定位、良恶性肿瘤的鉴别。若用131I标记的显像剂,则患者需要口服复方碘溶液以封闭甲状腺。注射标记抗体前要做皮肤过敏试验。注射抗体前静脉注射2~4mg地塞米松,或肌内注射25mg异丙嗪。将放射免疫显像图与肝实质显像图比较,在相当于原肝内放射性缺损区,可见明显的放射性浓聚则为阳性,反之则为阴性。有学者用131I-AFP抗体做原发性肝癌的定性诊断,但所报道的阳性率高低不一。用131I-抗人肝细胞癌抗体的放射免疫显像用于诊断原发性肝癌及其转移灶时,特异性更强。
(4)PET显像 原发性肝癌对18F-FDG的摄取呈多样性。Okazumi等观察了35例肝占位病变对18F-FDG的摄取,发现的肝内病灶分为3类型:A型,18 F-FDG摄取高于周围正常组织; B型,18 F-FDG摄取与周围正常组织相近;C型,18 F-FDG摄取低于周围组织或无摄取。A型表现见于所有的HCC和肝转移,但只有55%的HCC呈A型摄取,其余的HCC呈B、C型表现。HCC摄取呈多样性的原因是其细胞分化程度。部分HCC分化好,可以迅速清除摄入的18FFDG,在显像时表现为B型或C型。
PET对肝癌治疗后的疗效监测价值较大。介入治疗对于不能手术的肝肿瘤是有效的姑息性治疗手段。临床上有时在患者术前使用血管内栓塞,以降低肿瘤活性,使手术切除更容易、更安全。介入治疗后通过CT可以观察栓塞后碘油聚积的情况和肿瘤坏死后变化,但不能显示残存的肿瘤活性。根据国内经验,对肝癌治疗后的PET观察发现,介入治疗后肿瘤坏死部位呈C型,而在治疗灶周边出现高浓聚区者,随诊均证实有肿瘤复发。PET表现为A、B型者,病灶部位仍存在病灶组织,而C型中90%的肿瘤组织坏死,提示PET发现肿瘤活性比CT所见的瘤内碘油存留更准确。
除了过小的病灶18F-FDG摄取表现为假阴性外,几乎所有转移性肝癌都表现为高摄取(图9-20)。在国内一组14例转移性肝癌的研究中,PET共发现转移病灶19个,均为A型。相应的CT、MR I分别检测出11个和13个转移灶。
肝PET检查的假阳性主要见于肝脓肿、偶尔扩张的胆道或小胆管阻塞并发周围炎症,可以表现出类似转移灶的摄取;假阴性主要见于过小病灶,以及40%左右的高分化HCC。结合其他影像发现和对HCC摄取多样性的了解,是减少漏诊的必要条件。
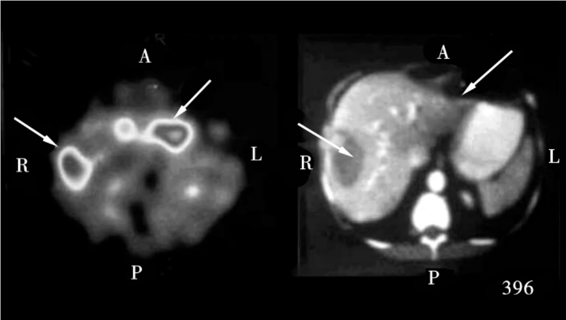
图9-20 肝肿瘤的8F-FDGPET-CT影像
图中所示早期可发现肝内的小肿瘤灶。
有关实用临床核医学诊疗技术的文章

静脉注入的放射性胶体颗粒约85%被库普弗细胞吞噬,从而使肝实质显影;其余15%则被脾和骨髓等的巨噬细胞摄取。根据肝内显像剂的分布状况,可以判断肝的位置、大小、形态以及有无占位性病变,从而达到诊断疾病的目的。2)99m Tc-植酸钠植酸钠本身不是胶体颗粒,而当它经静脉注入体内后,与血中钙离子螯合形成不溶性的99m Tc-植酸钙胶体,可以被肝的库普弗细胞吞噬而显像。......
2023-12-07

异位胃黏膜显像是诊断该病的特异检查方法。静脉注射99m后,异位胃黏膜很快聚集99m而呈现放射性浓聚影像,腹部除胃以外的其他部位则呈低放射性分布,据此可特异性地诊断梅克尔憩室的存在。当注射入99m后,被病变局部的异位胃黏膜壁细胞所摄取,故可显像而作出诊断。......
2023-12-07

将每个心动周期时段的放射性计数叠加起来,形成收缩期、舒张期不同时段的心肌灌注图像。常用的显像剂与心肌灌注相同。心率变化太大或心律不齐频繁者不宜做门控心肌灌注显像。3)可逆加不可逆性灌注缺损运动负荷或双嘧达莫介入显像出现局限性稀疏或缺损区,延迟显像原稀疏或缺损区范围缩小,见于心肌梗死伴缺血或严重缺血。......
2023-12-07

4)影像采集条件,一般分别于注射后1h、3h、6h、24h进行前位和后位全脑脊蛛网膜下隙显像。脑室显像一侧侧脑室注入显像剂后几分钟,除对侧侧脑室不显影外,全脑室系统均显影,并迅速到达基底池。脑脊液漏的诊断和定位CSF系统显像是检测和定位CSF漏理想而有效的方法,尤其是间断性CSF漏。......
2023-12-07

这种显像方式称为V/Q显像。V/Q显像方法包括以下几种。在不具备133Xe肺通气显像设备的核医学科,多采用这种V/Q显像方法。这种不匹配改变多见于急性肺动脉血栓栓塞、慢性肺动脉血栓栓塞、其他病因引起的肺栓塞、支气管肺癌、纵隔肺门占位以及其他胸肺肿瘤、肺动脉发育不全等患者,其V/Q显像也可呈不匹配改变。......
2023-12-07

随着PET-CT显像技术的成熟,骨代谢显像在临床上也开始得到广泛应用。目前,骨代谢显像主要用于鉴别肿瘤的良恶性和全身探测骨转移癌。在鉴别病灶性质方面,骨代谢PET显像有其长处,Dehdashti等报道20例伴骨骼病变的患者进行FDG-PET检查,采用SUV2.0作为判别阈值,可正确鉴别出14/15恶性病变和4/5例良性病变。评价治疗反应骨与软组织肉瘤的治疗常采用综合性治疗方案。......
2023-12-07

血池显像可见双侧肢体血池影像多数不对称,患侧放射性减低,患侧/健侧计数比值减小。出现坏疽时,血池显像可准确显示缺血范围,为手术切除提供依据。......
2023-12-07
相关推荐