随着科学技术和新兴工业的发展,对化学试剂的纯度、净度以及精密度的要求越来越严格,越来越专门化,因而出现了各种用途的专用试剂。(二)化学试剂的选用1.不同规格的化学试剂的纯度和杂质的含量都不相同,其价格相差也很大。试剂取出后应随手盖严瓶盖。......
2024-08-19
实验五 萃取
(一)实验目的
1.了解萃取的基本原理。
2.掌握萃取、干燥基本操作,学会分液漏斗的使用。
(二)实验原理
萃取是有机化学实验中用来提取或纯化有机化合物常用的操作之一。应用萃取可以从固体或液体混合物中提取出所需要的物质,也可以用来洗去混合物中少量杂质。通常前者称为“抽提”或“萃取”;后称者为“洗涤”。
萃取是利用物质在两种不互溶(或微溶)溶剂中溶解度或分配比的不同来达到分离、提取或纯化目的的一种操作。
萃取的主要理论依据是分配定律。物质在不同的溶剂中有着不同的溶解度,这可用与水不互溶(或微溶)的有机溶剂从水中萃取有机化合物来说明。将含有机化合物的水溶液用有机溶剂萃取时,有机化合物就在两液相间进行分配。在一定温度下,此有机化合物在有机相中和在水相中的浓度比为一常数,此即所谓“分配定律”,用公式表示cA/cB=K。
式中cA、cB分别表示一种化合物在两种互不相溶的溶剂中的物质的量浓度。K是一个常数,称为“分配系数”。它可以近似地看作此物质在两溶剂中溶解度之比。
有机物质在有机溶剂中的溶解度,一般比在水中的溶解度大,所以可以将它们从水溶液中萃取出来。但是除非分配系数极大,否则一次萃取是不能将全部物质移入新的有机相中的。在萃取时,若在水溶液中先加入一定量的电解质(如NaCl),利用所谓“盐析效应”以降低有机化合物和萃取剂在水中的溶解度,常可提高萃取效果。
当用一定量的溶剂从水溶液中萃取有机化合物时,一次萃取好呢还是多次萃取好呢?
设在Vml水中溶解W0g物质,每次用Sml与水不互溶的溶剂重复萃取,假如W1g为萃取一次后剩留在水溶液中的物质量,则在水中的浓度和在有机相中的浓度分别为W1/V和(W0-W1)/S二者之比等于K,亦即
则萃取两次后在水中的剩留量W2则有
显然萃取n次后的剩留量Wn应为
因为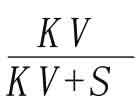 恒小于1,所以n越大,Wn就越小,也就是说把溶剂分成几份作多次萃取比用全部量的溶剂作一次萃取为好。
恒小于1,所以n越大,Wn就越小,也就是说把溶剂分成几份作多次萃取比用全部量的溶剂作一次萃取为好。
但必须注意,上面的式子只适用于几乎和水不互溶的溶剂。对于与水有少量互溶的溶剂,上面的式子只是近似的但也可以定性地提出预期的结果。
萃取率为萃取液中被萃取物质与原溶液中该物质物质的量之比。萃取率越高,表示萃取过程的分离效果越好。
(三)实验操作
1.液-液萃取。
(1)选择仪器:在实验中用的最多的是水溶液中物质的萃取。最常用的萃取器皿为分液漏斗。操作时应选择容积较液体体积大一倍以上的分液漏斗。
(2)器密性检查:擦干分液漏斗、活塞及塞孔,在离活塞孔稍远处薄薄地涂上一层润滑脂(注意切勿涂得太多或使润滑脂进入活塞孔中,以免玷污萃取液),塞好活塞后再把活塞旋转几圈,使润滑脂均匀分布,看上去透明即可。
(3)查漏:一般在使用前,应在漏斗中放入水摇荡,检查塞子与活塞是否渗透漏,确认不漏水时方可使用。
(4)然后将漏斗放在固定在铁架台上的铁圈中,关好活塞,将要萃取的水溶液和萃取剂(一般为溶液体积的1/3)依次自上口倒入漏斗中,塞紧塞子(注意塞子不能涂润滑脂)。
(5)萃取:取下分液漏斗,用右手掌顶住漏斗顶塞并握住漏斗,左手握住漏斗活塞处,大姆指压紧活塞,把漏斗放平,前后振摇(见图2-8a)。在开始时振摇要慢。摇振几次后,将漏斗的上口向下倾斜,下部支管向斜上方(朝向无人处),左手仍握在活塞支管处,用姆指和食指旋开活塞,通过指向斜上方的支管释放出漏斗内的压力,也称“放气”(见图2-8b)以乙醚萃取水溶液中的物质为例,在振摇后乙醚可产生40kPa~66.7kPa的蒸气压,加上原来的空气和水蒸气压,漏斗中的压力就大大超过了大气压。如果不及时放气,塞子就可能被顶开而出现喷液。待漏斗中过量的气体逸出后,将活塞关闭再进行振摇。如此重复至放气时只有很小压力后,再剧烈振摇2min~3min,然后将漏斗放回铁圈中静置,使两液分层,旋转上面玻璃塞,对好放气孔,再将下面活塞缓缓旋开,使下层液从活塞放出。上层液从分液漏斗上口倒出,切不可从活塞放出。以免被残留在漏斗颈上的第一种液体所玷污。分液时一定要尽可能的分离干净。有时在两液相之间可能出现一些絮状物,也应同时放出。将水溶液倒回分液漏斗中,再用新的萃取剂萃取。萃取次数取决于分配系数,一般为3~5次,将所有的萃取液合并,加入适当干燥剂进行干燥,然后蒸去溶剂,萃取所得的有机物视其性质再确定其纯化方法。
图2-8 分液漏斗的振摇
上述操作中的萃取剂是有机溶剂,它是根据“分配定律”使有机化合物从水溶液中被萃取出来。另外一类萃取原理是利用它能与被萃取物质起化学反应,这种萃取通常用于从化合物中移去少量杂质或分离混合物。操作方法与上面相同。常用的这类萃取剂如5%氢氧化钠水溶液,5%或10%的碳酸钠水溶液、碳酸氢钠水溶液,稀盐酸、稀硫酸及浓硫酸等。碱性的萃取剂可以从有机相中移出有机酸,或从溶于有机溶剂的有机化合物中除去酸性杂质(使酸性杂质形成钠盐溶于水中)。稀酸可从混合物中萃取出有机碱性物质或用于除去碱性杂质。浓硫酸可应用于从饱和烃中除去不饱和烃,从卤代烃中除去醇及醚等。(www.chuimin.cn)
萃取某些含有碱性或表面活性较强的物质时,常会产生乳化现象,有时由于存在少量轻质的沉淀、或溶剂部分互溶,或两液相相对密度相差较小等原因,都会使两液相不能很清楚地分开。破坏乳化的方法有:①较长时间静置;②若两种溶剂能部分互溶而发生乳化现象,可加入少量电解质(如氯化钠),利用盐析作用加以破坏,在两相相对密度相差很小时加入氯化钠也可增加水相的相对密度;③若因碱性物质产生乳化现象,常加入少量稀硫酸或采用过滤等方法来消除;④加热也可破坏乳状液(注意防止燃烧),或滴加数滴醇改变表面张力,以破坏乳状液。
萃取溶剂的选择,应随被萃取化合物的性质而定(如分配系数、密度、沸点等)。一般水溶性较小的物质可用石油醚萃取;水溶性较大的可用苯或乙醚;水溶性极大的用乙酸乙酯等。
2.%液-固萃取
固体物质的萃取,通常是用长期浸出法或采用脂肪提取器(索氏提取器)。前者是靠溶剂长期的浸润溶解而将固体物质浸出来。这种方法不需要任何特殊器皿,但效率不高而且溶剂所需量较大。脂肪提取器(图2-9)是利用溶剂回流及虹吸原理,使固体物质连续不断地被纯的溶剂所萃取,因而效率较高。
图2-9 脂肪提取器
(四)〖实验〗用萃取法分离一种二组分混合物
实验室现有对甲苯胺和荼两组分混合物,依据其性质和溶解度,设计合理方案将各组分离出来。
1.分别用量筒量取50mL水和6mLHCl(浓)配制成稀盐酸溶液,并将其分成两等份分别盛放在烧杯中备用。
2.称取2克对甲苯胺和萘的混合物,使其溶解于20ml乙醚中。
3.将上述乙醚溶液用1中配制的盐酸溶液萃取两次。
4.收集乙醚萃取液用水洗一次,并将水洗液与上两次萃取后的水溶液合并。乙醚溶液用CaCl2干燥。
5.将水层用10%NaOH中和直至碱性为止。充分冷却,然后,将析出的晶体进行抽滤,洗涤晶体,充分干燥后,计算收率,并测熔点。
6.将4中充分干燥后的乙醚滤入干燥的圆底烧瓶中水浴进行蒸馏,回收乙醚后得到萘的晶体,充分干燥后称重同时测定其熔点。
必要时,每种组分可进一步重结晶,以获得熔点敏锐的纯品。
注意事项
1.使用分液漏斗时,应注意:
a.使用前检查玻璃塞和活塞是否紧密,漏不漏水;
b.不能把分液漏斗放入烘箱中烘干;
c.使用分液漏斗时,记住经常放气,避免内压过高。解除压力时,漏斗支管不能指向人。
2.萃取操作中,均用小口带塞的锥形瓶,减少有机溶剂挥发。
(五)思考与讨论
1.使用分液漏斗应注意哪些事项?
2.怎样判断有机层在上层还是在下层?若用下列溶剂萃取水溶液,它们将在上层还是在下层?
乙醚、苯、氯仿
3.在蒸馏回收乙醚时应注意什么问题?
有关基础化学实验.1, 有机化学实验模块的文章

随着科学技术和新兴工业的发展,对化学试剂的纯度、净度以及精密度的要求越来越严格,越来越专门化,因而出现了各种用途的专用试剂。(二)化学试剂的选用1.不同规格的化学试剂的纯度和杂质的含量都不相同,其价格相差也很大。试剂取出后应随手盖严瓶盖。......
2024-08-19

实验二十一乙酰水杨酸的制备(一)实验目的1.学习以酚类化合物作原料制备酯的原理和实验方法。本实验将利用前一个反应制备乙酰水杨酸。在生成乙酰水杨酸的同时,水杨酸分子之间可以发生缩合反应,生成少量的聚合物。水杨酸可与三氯化铁形成深色络合物,而纯净的乙酰水杨酸因酚羟基已被酰化,不再与三氯化铁发生类似颜色反应,因此杂质很容易被检出。将滤液冷却至室温使乙酰水杨酸晶体析出。......
2024-08-20

实验十七苯乙酮的制备(一)实验目的1.学习并掌握傅-克酰基化反应的基本原理。沸水浴上回流20min,直至无氯化氢气体放出。注意事项1.所用仪器必须干燥,称取和加入AlCl3时应快速。......
2024-08-20

实验二十二8-羟基喹啉的制备(一)实验目的1.学习合成8-羟基喹啉的原理和方法。本实验以邻氨基苯酚、邻硝基苯酚、无水甘油和浓硫酸为原料经Skraup反应合成8~羟基喹啉。纯粹8-羟基喹啉的熔点为75℃~76℃。......
2024-08-20

实验二十九微波辐射合成肉桂酸(一)实验目的1.了解微波辐射条件下合成肉桂酸的原理和方法。(二)实验原理本实验是在微波炉中进行常压反应,将反应物和溶剂放入常法所用的玻璃器皿中,装上常法装置,反应物和溶剂吸收微波能量后升温,并发生反应。纯肉桂酸(反式)为白色片状结晶,熔点133℃。注意事项无水醋酸钾需新鲜烧焙。水是极性物质能强烈吸收微波,影响反应吸收微波效率。......
2024-08-20

实验三薄层色谱和纸色谱(一)实验目的1.了解色谱法的基本原理及薄层层析和纸层析的用途。此外,薄层色谱法还可用来跟踪有机反应及进行柱色谱之前的一种“预试”。纸色谱(纸层析)属于分配色谱的一种,主要用于多官能团或高极性化合物如糖、氨基酸等的分离。......
2024-08-20

Ⅲ危险化学药品的使用与保存化学工作者经常使用各种各样的化学药品进行工作。根据常用的一些化学药品的危险性,大体可分为易燃、易爆和有毒三种,现分述如下。这种情况不多,为防止中毒,任何药品不得用口尝味,严禁在实验室进食,试验结束后必须洗手。无机化学药品①氰化物及氢氰酸:毒性极强、致毒作用极快,空气中氰化氢含量达到万分之三,数分钟内即可致人死亡,使用时须特别注意。......
2024-08-20

实验二十五肉桂酸乙酯的合成及用1HNMRJ鉴定顺反异构(一)实验目的1.掌握酯缩合反应的原理及合成技能。所以只要测出两种异构体双键的耦合常数就很容易确定其结构。称量产量,计算产率。取约30mg固体样加入另一支核磁品管中,用0.5mLCDCl3溶解,加入1滴TMS。......
2024-08-20
相关推荐