【摘要】:两种缓蚀剂对金属缓蚀行为的电化学研究武汉东湖学院生命科学与化学学院王莹莹,彭灵波,张铁雄,安从俊,宋昭华本文采用电化学工作站,对在不同浓度的盐酸与缓蚀剂溶液中的碳钢电极的缓蚀行为进行了研究。金属腐蚀不仅带来巨大的经济损失,而且往往会带来人生安全和环境污染等事故。国内也有科研工作者在探索绿色缓蚀剂氨基酸在抑制金属腐蚀方面的应用。将称取的缓蚀剂溶于上述制好的盐酸溶液中制成相对应的缓蚀剂—腐蚀液体系。
两种缓蚀剂对金属缓蚀行为的电化学研究
武汉东湖学院生命科学与化学学院
王莹莹,彭灵波,张铁雄,安从俊,宋昭华
本文采用电化学工作站,对在不同浓度的盐酸与缓蚀剂溶液中的碳钢电极的缓蚀行为进行了研究。实验结果表明:十二烷基磺酸钠的缓蚀效率变化不大,其缓蚀效率均在85%左右,起到了较好的缓蚀效果;而乌洛托品的缓蚀效率变化随着盐酸浓度的变化则较为显著,当盐酸浓度为0.01mol/L时,其缓蚀效率为80%左右,而当盐酸浓度增加为0.05mol/L时,其缓蚀效率降到50%左右。
一、前言
种类繁多的金属材料已成为人类社会发展的重要物质基础,而金属制品在生产和使用中,也不可避免的要受到各种损坏,如机械磨损、生物性破坏、腐蚀等。金属腐蚀是金属在环境的作用下所引起的破坏或变质。据统计,全世界每年因腐蚀而报废的钢铁占年产量的30%,我国每年生产的钢铁有20%用于替换那些因腐蚀而丧失用途的产品。金属腐蚀不仅带来巨大的经济损失,而且往往会带来人生安全和环境污染等事故。
近年来,缓蚀剂的研究方向是研究不同缓蚀剂在不同体系中复配的情况下对金属材料的保护性能。随着环保意识的不断提高,人们现在已经开始逐步淘汰落后的缓蚀工艺与药品。现在已经有人开始从天然植物如桉树叶和其他一些植物中提取有缓蚀效果的物质,国外有人在酸性植物提取液体系中研究金属腐蚀的电化学行为,并取得了一定的效果。国内也有科研工作者在探索绿色缓蚀剂氨基酸在抑制金属腐蚀方面的应用。
二、实验部分
(一)实验仪器及药品
仪器:RST5200电化学工作站(郑州世瑞思仪器科技公司),电极(自制的碳钢电极)
药品:盐酸 氢氧化钠 邻苯二甲酸氢钾(试剂均为分析纯)
(二)实验方法
(1) 标定盐酸溶液浓度
(2)按实验所需缓蚀剂的浓度,计算缓蚀剂的用量,然后准确按量称取缓蚀剂。将称取的缓蚀剂溶于上述制好的盐酸溶液中制成相对应的缓蚀剂—腐蚀液体系。
(3)开启RST-5200电化学工作站,预热10分钟。同时,对工作电极进行预处理,包括用砂纸对其表面进行打磨等处理,确保电极表面洁净光滑。
(4) 设定好实验参数,开始实验,记录数据并绘制塔菲尔图。
(5)进行平行实验,重新对电极表面进行处理,并更换与(2)中浓度缓蚀剂—腐蚀液体系。再按步骤(4)(5)重复两次。
三、结果与讨论
(一)碳钢电极表面产生极化最佳条件的选择
1.扫描速度对塔菲尔图的影响
固定反应体系的浓度、温度等条件,以扫描速度为单一变量,分别设定扫描速度为0.03V/s、0.02V/s、0.0008V/s,来研究扫描速度对塔菲尔图的影响,所得结果见图1。
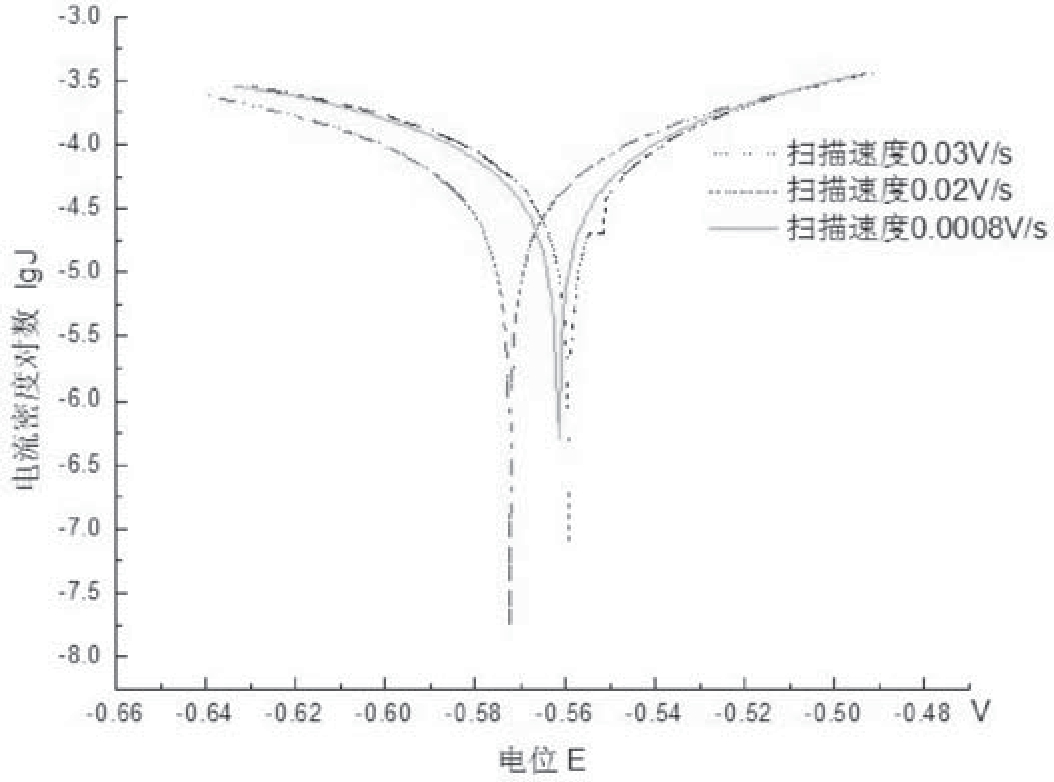
图1 不同扫描速度对塔菲尔图形的影响
从图1可知,在阳极极化阶段,即图形右支,lgJ随着电位E的增加而增大。但当扫描速度为0.03V/s时,当电位从—0.554V增大到—0.551V范围内时,lgJ不随E的增大而改变,而是呈与横坐标平行的停滞阶段。而当扫描速度小于0.03V/s时,则上述情况并未出现。由上述分析可知,当外加电压随时间变化越大,即扫描速度越大时,电极表面电位的变化越大,电极表面甚至来不及发生腐蚀,从而导致该现象的产生。
2.采样间隔对塔菲尔图的影响
固定反应体系的浓度、温度等条件,以扫描速度为单一变量,分别设定采样间隔0.0001V、0.0002V、0.001V、0.002V,来研究扫描速度对塔菲尔图的影响,所得结果见图2。
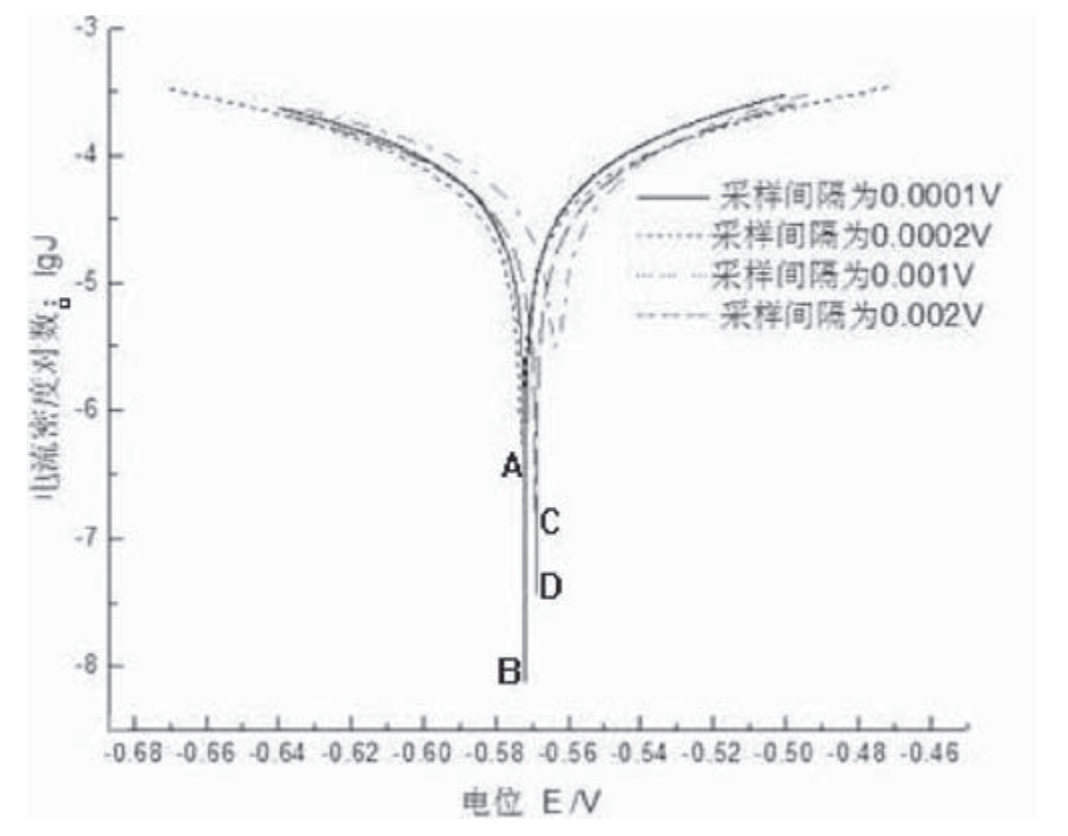
图2 不同采样间隔对图形的影响
由图2可知,采样间隔越小,相同电位范围内所测得的数据点越多,所测得的数据就越准确。采样间隔越小,电极由阴极极化转变为阳极极化瞬间的电流密度对数lgJ越准确,即图形中反映出的纵坐标lgJ峰值越明显,如图2所示,即AB段比CD段长度长,峰值更明显。当采样间隔不超过0.0002V时,lgJ峰值较为明显;当采样间隔大于0.001V时,电极由阴极极化转变为阳极极化时瞬间的电流密度对数lgJ的峰值并不明显。(www.chuimin.cn)
综上所述,在仪器响应时间的允许范围内,最佳的反应条件为扫描速度小于0.007V/s,采样间隔不大于0.0002V。本实验中扫描速度为0.004V/s,采样间隔为0.0001V。
(二)十二烷基磺酸钠对腐蚀速度的影响
固定其他条件,使缓蚀剂浓度为单一变量,研究在不同浓度十二烷基磺酸钠溶液中盐酸溶液对碳钢电极的腐蚀。在下列实验条件下进行实验:
A.实验环境为盐酸浓度0.01mol/L,扫描速率0.004V/s,采样间隔 0.0001V,温度25℃,恒温水浴。结果见图3。
B.实验环境为盐酸浓度0.05mol/L,扫描速率0.004V/s,采样间隔 0.0001V,温度25℃,恒温水浴。结果见图4。
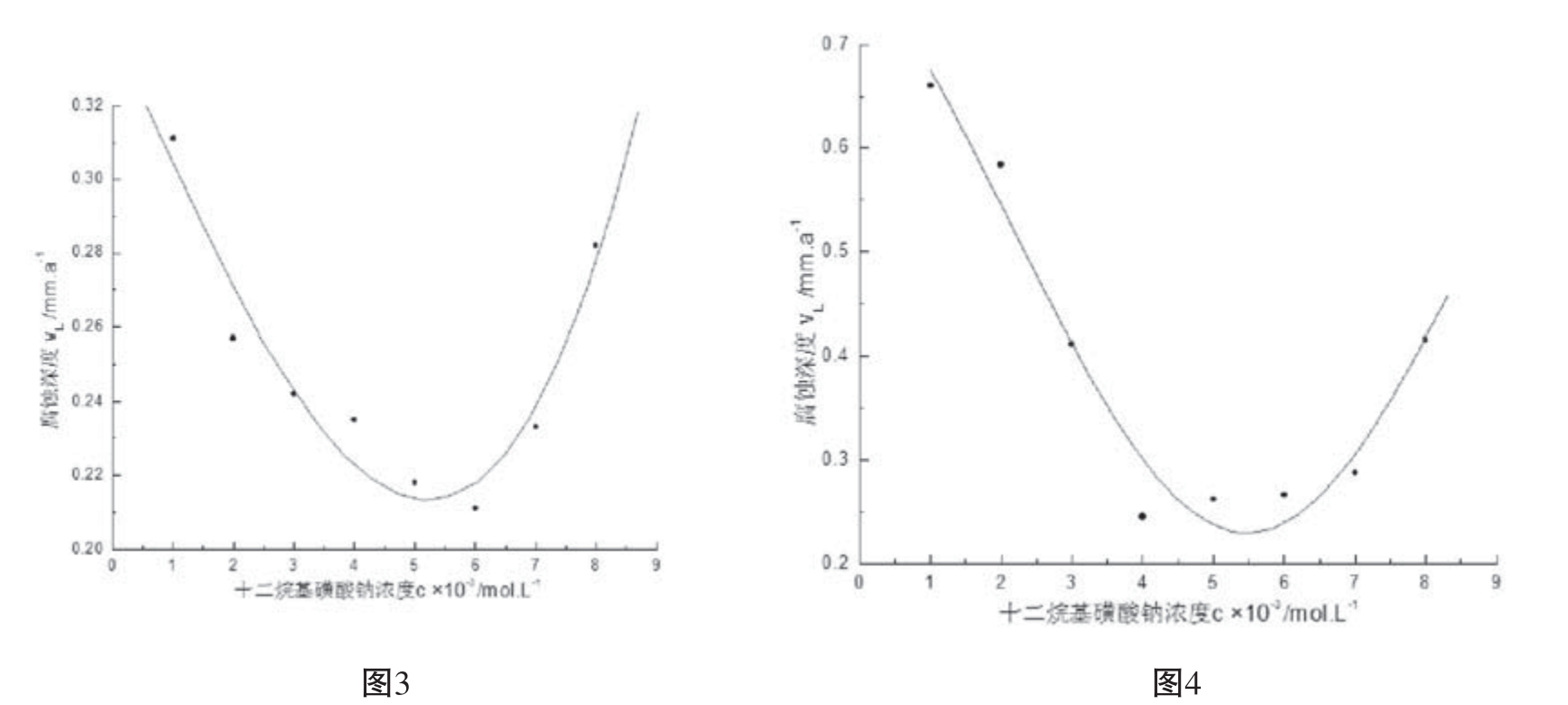
不同浓度十二烷基磺酸钠溶液中碳钢电极的腐蚀深度
由图3可知,当十二烷基磺酸钠浓度为0.001—0.005mol/L时,可以看出其腐蚀深度在减小,浓度从0.005mol/L升到0.008mol/L时,腐蚀深度逐渐增大。这主要是因为十二烷基磺酸钠是表面活性剂,当其浓度较小时,溶液中胶粒数较少,不能在工作电极表面形成完整的保护膜,致使腐蚀液与工作电极表面之间并没有形成良好的保护界面,此时,缓蚀剂虽能在一定程度上对工作电极进行保护,但远没有达到最大的保护程度;而当十二烷基磺酸钠浓度过大时,溶液中的胶粒形成胶束,所以溶液中的胶粒并未完全在电极表面形成良好的保护膜,从而导致了随着缓蚀剂浓度增加,腐蚀深度相反还增大的原因。
综上所述,当盐酸浓度为0.01mol/L时,十二烷基磺酸钠的最佳缓蚀浓度在0.005—0.007mol/L之间。通过计算得出其最佳缓蚀为84%左右。
将图3与图4对比,进行分析可发现在不同浓度的盐酸溶液中,缓蚀剂十二烷基磺酸钠的最佳缓蚀浓度有所增加,但增加量较小,缓蚀剂的缓蚀效率为88%左右。考虑到实验中误差的影响,可认为缓蚀剂最佳缓蚀浓度与缓蚀效率其基本上无变化,曲线走势与图4一样。但在不同浓度的盐酸溶液中,当未加入缓蚀剂的时候,在0.01mol/L的盐酸溶液中,工作电极的腐蚀深度为1.351mm/a,而在0.05mol/L的盐酸溶液中,工作电极的腐蚀深度为2.215mm/a,说明无缓蚀剂时,随着盐酸浓度增加,腐蚀深度增大。而当加入十二烷基磺酸钠之后,对在缓蚀剂浓度相同而盐酸溶液浓度不同时所得到的数据进行比较,可以发现两者的腐蚀深度在接近缓蚀剂最佳缓蚀浓度时无太大变化,说明缓蚀剂在此浓度范围内起到了缓蚀作用。
(三)乌洛托品对腐蚀速度的影响
固定其他条件,使缓蚀剂浓度为单一变量,观测在不同浓度乌洛托品溶液中盐酸溶液对碳钢电极的腐蚀。在下列实验条件下进行实验:
C.实验环境为盐酸浓度0.01mol/L,扫描速率0.004V/s,采样间隔 0.0001V,温度25℃,恒温水浴。结果见图5。
D.实验环境为盐酸浓度0.05mol/L,扫描速率0.004V/s,采样间隔 0.0001V,温度25℃,恒温水浴。结果见图6。

图5 不同浓度乌洛托品中电极腐蚀深度关系图
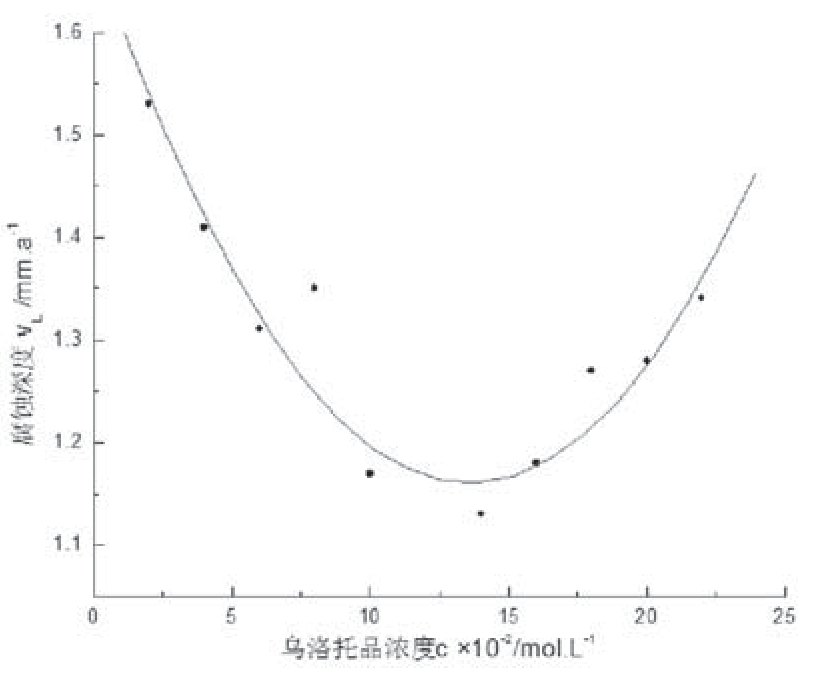
图6 不同浓度乌洛托品中电极腐蚀深度
由图5可知,当乌洛托品浓度在0.16—0.20mol/L时缓蚀效果最佳,此时缓蚀剂的最佳缓蚀效率在83%左右。当乌洛托品的浓度小于0.16mol/L时,所形成胶粒无法完全覆盖在电极表面,从而无法在最大程度上保护电极;当浓度过大时,乌洛托品胶粒形成胶束,不能在电极表面形成完整的保护膜,同时也造成了乌洛托品的浪费。
由图6可知,当乌洛托品浓度在0.16—0.20mol/L时缓蚀效果最佳,最佳缓蚀效率在50%左右。
通过图9与图10对比可发现,乌洛托品在不同浓度的盐酸溶液中最佳缓蚀浓度有较明显的变化,而且随着溶液中酸度的增加,腐蚀深度明显变大,缓蚀效率迅速下降。当盐酸浓度为0.01mol/L时,其缓蚀效率在83%左右,而当盐酸浓度为0.05mol/L时,缓蚀效率迅速下降至50%左右。这说明乌洛托品在酸性环境下,缓蚀性能随着酸度的变化而变化。
四、结论
十二烷基磺酸钠在不同的酸性环境下,其最佳缓蚀浓度与缓蚀效率并未有明显的影响,其缓蚀效率均在80%以上,有效地抑制了电极表面的腐蚀;但乌洛托品在不同的酸性环境下,其最佳缓蚀浓度均出现了较大变化,在0.01mol/L的盐酸溶液中,其缓蚀效率能达到83%,能够较好地抑制腐蚀的发生,而当盐酸浓度增大到0.05mol/L时,其缓蚀效率下降到50%左右,缓蚀效果明显降低。这也说明了在酸性环境下,十二烷基磺酸钠的缓蚀性能和缓蚀效果比乌洛托品强。
【参考文献】
[1]庞雪辉.酸性条件下环境友好型缓蚀剂缓蚀性能及机理的研究[D].青岛:中国海洋大学,2007.
[2]张玉梅.关于钢铁氧化处理和磷化处理的实验研究及应用[J].辽宁师专学报,2003,5(1):103—105.
[3]RAJA Pandian Bothi,RAHIMAfidah Abdul,OSMAN Hasnah ect. Inhibitory Effect of Kopsia Singapurensis Extract on the Corrosion Behavior of Mild Steel in Acid Media[J].Acta Phys.Chim.Sin,2010,26(8):2171—2176.
[4]吴伟明,杨萍,杜海燕等. 绿色缓蚀剂氨基酸在抑制金属腐蚀方面的应用[J].表面技术,2006,35(6):51—53.












相关推荐