对吴淞江流域远古文化遗址发掘、出土的文物进行分析,我们发现,当时先民的经营活动已经有明确的分工,其手工生产已经分出纺织、制陶和琢玉等门类,甚至还有酿酒,而且其工艺都达到一定的先进水平。在三四千年前的吴淞江流域的先民们竟然已经能够制作出精美的漆器了!总的来说,吴淞江流域的良渚文化时期的玉器形状和纹饰都是形式多样,工艺先进的。上面,笔者简要叙述了吴淞江流域远古文化中先进的手工业。......
2023-11-18
工业硫酸亚铁的提纯工艺研究
本文以工业硫酸亚铁为原料,采用酸浸—还原—除杂—冷却结晶—干燥的工艺,制取医药级的硫酸亚铁。我们通过实验确定最佳的置换温度为60℃、初始PH值为2.8、置换反应时间为3h,并考虑滤液的循环使用,确定最佳的循环次数为1次;提纯的硫酸亚铁纯度达99%以上,钛离子含量低于0.0139%。
一、前言
七水硫酸亚铁(FeSO4·7H20)俗称绿矾,为淡蓝绿色晶体,分子量为278.03,比重为1.895—1.898。七水硫酸亚铁在干燥的空气中可风化脱水,生成白色的硫酸亚铁粉末;在湿空气中易氧化,生成棕黄色碱式硫酸铁。
钛白粉是一种重要的无机染料,我国大多数厂家均采用硫酸法制造。一般,每生产1吨钛白粉,副产硫酸亚铁3.5—4.0吨。钛白生产副产物废渣绿矾除含亚铁盐外,还含有Ti、Mg、Mn、Al、Si、Cu等各种杂质,不能直接利用,而且随地堆放不仅会严重污染环境,还造成资源的浪费。高纯度硫酸亚铁是制备超细氧化铁、磁性材料、氧化铁黄、饲料添加剂等的重要原料,随着工业的发展,对高纯度硫酸亚铁的需求量也越来越大。如何去除钛白副产物中的杂质,实现经济效益和社会效益的双重效益,也受到越来越多关注。
本实验以钛白副产物粗绿矾为原料,以最终产品达到医药级硫酸亚铁为目标,通过分析原料和产品中硫酸亚铁和钛质量含量的变化(表1),研究了酸浸时的最佳反应温度、初始pH值、最佳反应时间等因素的影响;同时为了减少废水的排放,探讨了滤液的循环使用次数的影响。
表1 医药级硫酸亚铁中FeSO4·7H2O和钛含量指标[3]
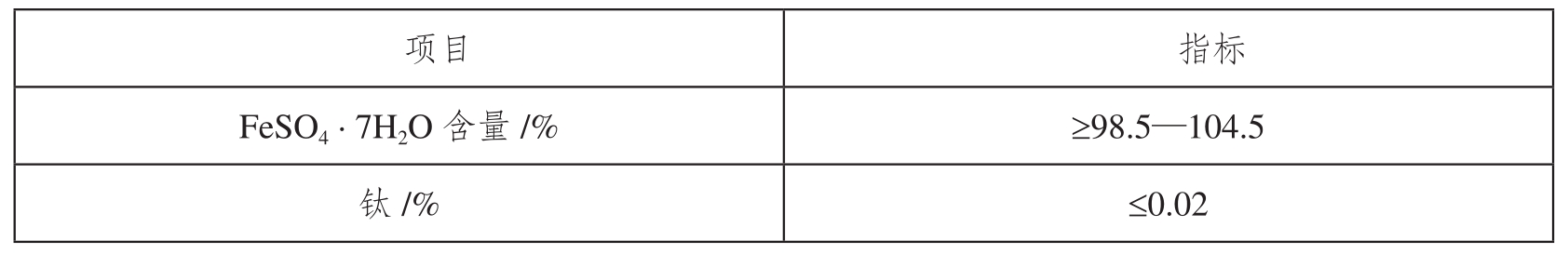
二、实验材料与方法
(一)实验仪器、试剂和材料
实验仪器:pH计,恒温水槽,紫外可见分光光度计(sp-1901,上海)等。
试剂包括硫酸,磷酸,聚丙烯酰胺,过氧化氢,还原铁粉,二氧化钛,硫酸铵,高锰酸钾等。(以上药品均为分析纯)
硫酸亚铁:工业级,主要成分见表2。
表2 原料用工业硫酸亚铁主要成分表
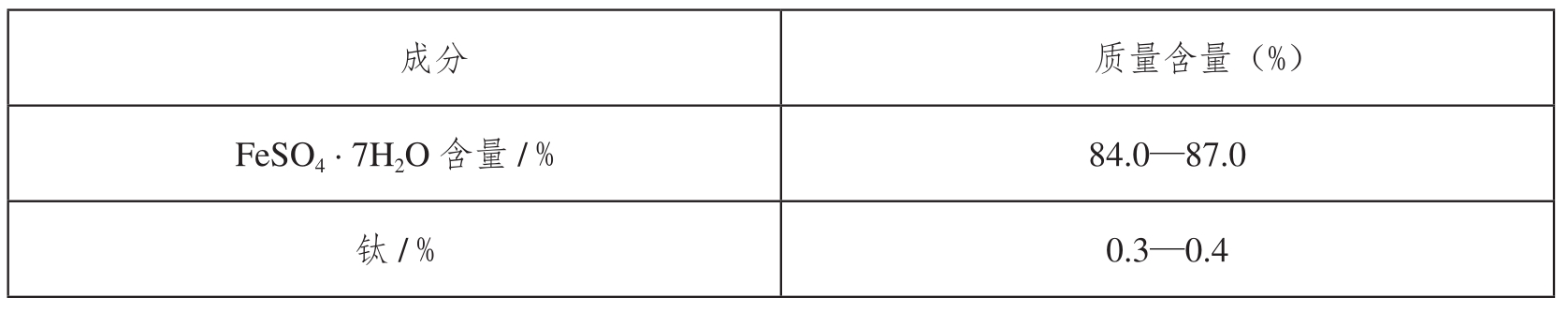
(二)实验方法
称取适量的工业硫酸亚铁与三口烧瓶中,溶液浓度为70g/L,加入硫酸调节溶液的pH=2.8,向其中加入工业硫酸亚铁质量1%的还原铁粉,恒温反应,控制反应温度在70℃—90℃。
水解完全后,趁热抽滤。将滤液趁热转入干净的三口烧瓶中,加入少量絮凝剂(聚丙烯酰胺),通入氧气,恒温50℃搅拌10min。趁热抽滤。
将滤液转入烧杯中,放冷至室温后,放入冰水浴中结晶。结晶后过滤、干燥。实验工艺流程图如图1。
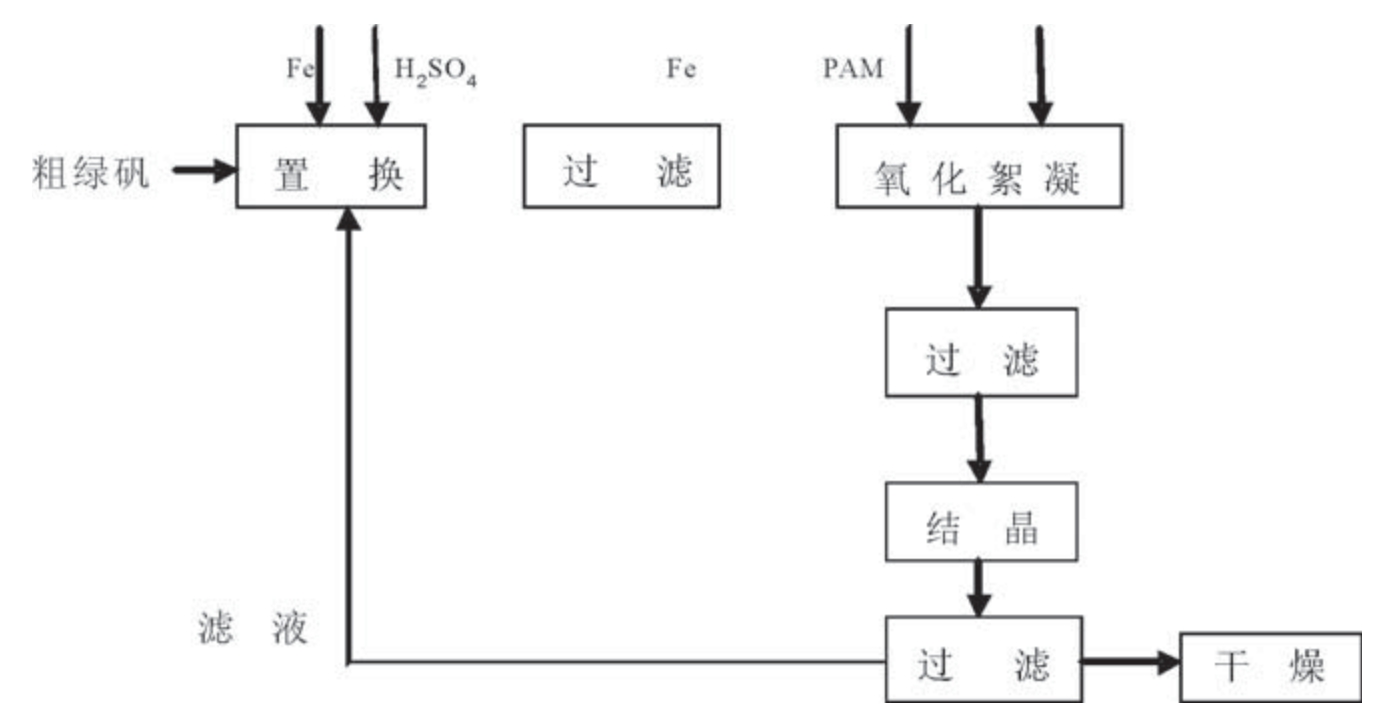
图1 硫酸亚铁提纯工艺流程图
(三)分析方法
1.高锰酸钾滴定法测Fe2+含量
准确称取一定量(m)试样,置于250ml锥形瓶中。用50ml水溶解,加入10ml1:1硫酸和4ml1:1磷酸。以C(1/5KMnO4)约0.1mol/l标准溶液滴定至终点,记录消耗标准溶液体积V。计算公式如下:
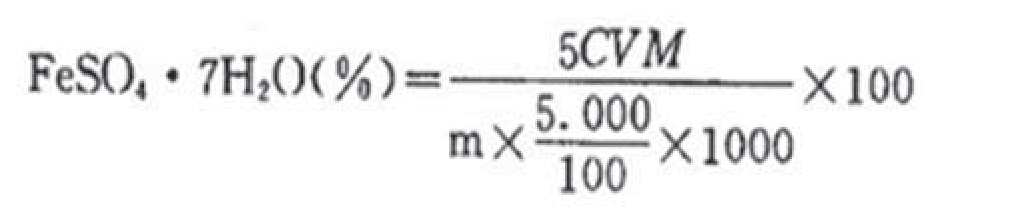
2.紫外可见分光光度法测Ti2+含量
配制0.2mg/ml的钛标准溶液。用紫外分光光度计测量钛离子的含量然后与TiO2标准曲线进行对比,TiO2标准线见图2所示。
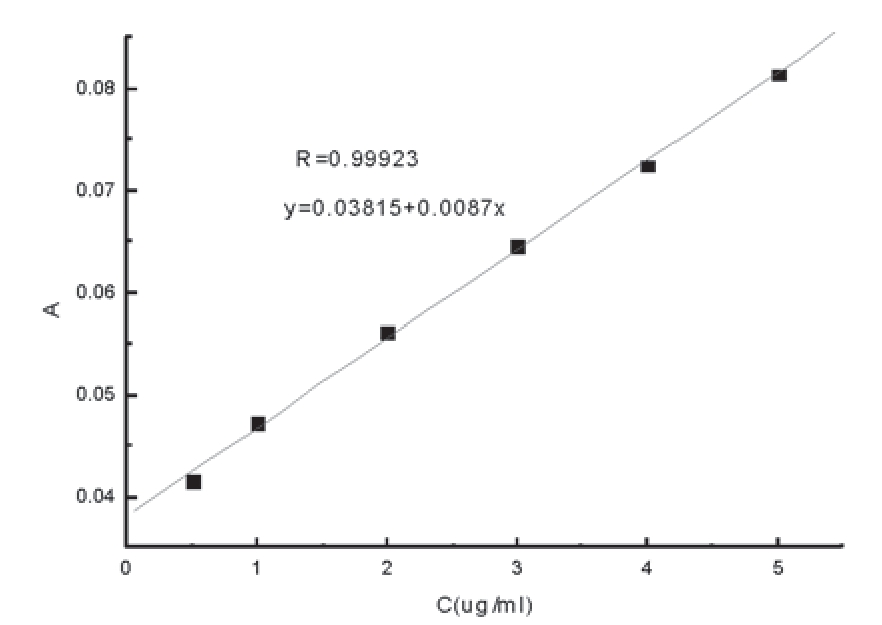
图2.Tio2标准曲线(www.chuimin.cn)
三、实验结果讨论及分析
(一)反应时间对产品纯度的影响
通过控制反应温度为70℃,pH=2—3,测定不同反应时间对产品纯度的影响。结果如图3所示。
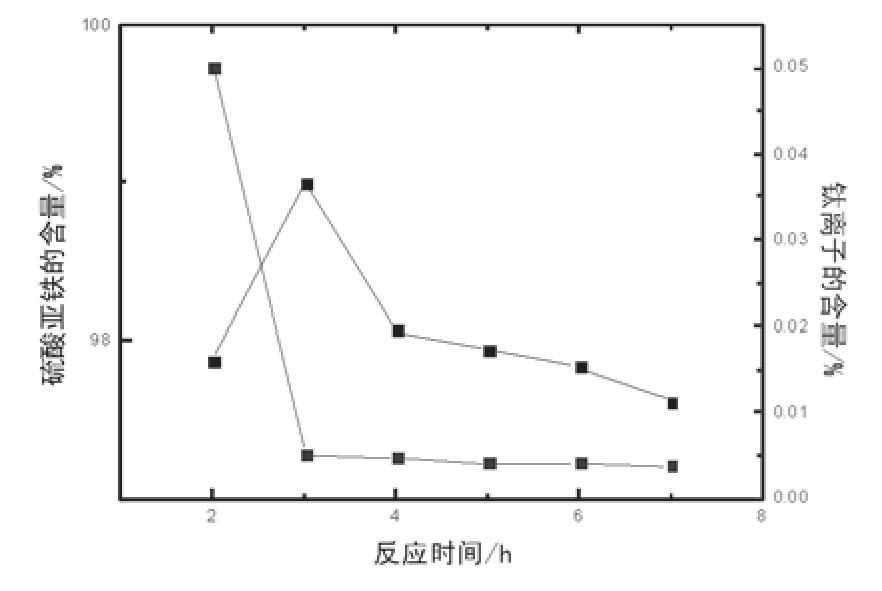
图3.反应时间对产品纯度的影星
由图3知,反应时间为3h时,FeSO4·7H2O质量含量在医药级范围内。因此选择反应时间为3h。
(二)反应温度对产品纯度的影响
通过控制反应时间为3h,PH=2—3,测定不同反应温度对产品纯度的影响。结果见图4。
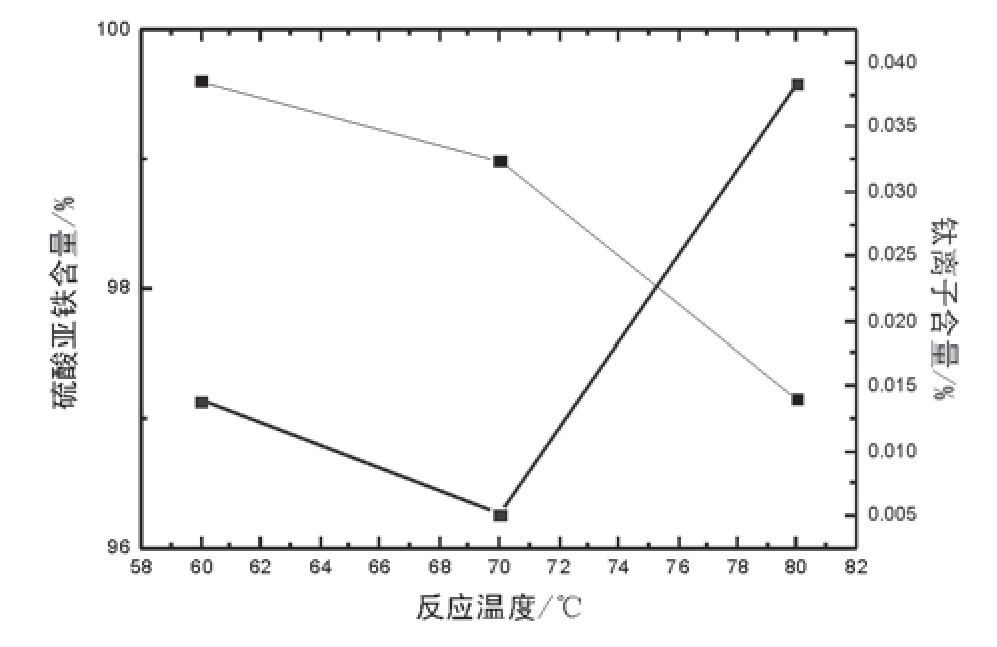
图4.反应温度对产品纯度的影响
由图4可知,随着反应温度上升,产品中硫酸亚铁质量含量下降,而钛离子含量则在70℃以上时不降反升,综合考虑后确定反应温度为60℃。
(三)反应溶液初始pH值对产品纯度的影响
通过控制反应温度为60℃,反应时间为3h,测定不同pH对产品纯度的影响。结果如图5所示。

图5.初始pH对产品纯度影响
由图5知,pH值为2.8时产品中硫酸亚铁含量最高,而钛含量较低。因此选择反应溶液的初始pH值为2.8。
(四)滤液的循环使用次数
表3 滤液的循环次数对产品纯度的影响
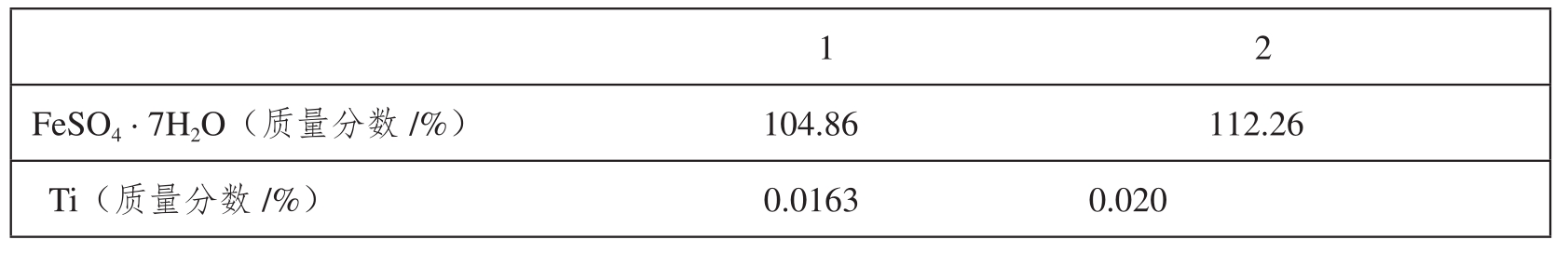
由表3知,当滤液循环使用2次时,产品中钛含量超过0.02%。因此滤液可以循环使用1次。再次使用时可将滤液先进行稀释,然后再进行使用。
四、结语
利用此流程提纯硫酸亚铁,最佳的反应温度为60℃,反应时间为3h,初始pH为2.8。通过该流程使制取的硫酸亚铁的纯度达到99%以上,钛离子的含量低于0.0139%,上述指标达到医药级硫酸亚铁规定的标准。滤液可循环使用一次。
本实验中对结晶过滤后的滤液直接使用,未经过稀释,因此由于滤液浓度过大,只能使用一次。可考虑将滤液稀释再进行使用,这样就可以循环使用多次,从而减少废水排放量。
【参考文献】
[1] 席美云,张克立,余幼租等.湿化法制备超细氧化铁的研究[J].化学世界,1992,(4):183—186.
[2] 宁云金,王统理.用副产硫酸亚铁生产优质氧化铁[J].应用化工,2005,34(10):653—655.
[3] 谢全模,胡文方,张莉等.废渣绿矾精制高纯度硫酸亚铁的研究[J].河南化工,2007,24(11):33—35.
[4] 水处理剂.硫酸亚铁[S],中国,2006,GB10531-2006.
[5] 罗敏.紫外可见分光光度法测定聚酯纤维中二氧化钛含量[J]河北化工,1991,(1):144—146.
有关武汉东湖学院论文集的文章

对吴淞江流域远古文化遗址发掘、出土的文物进行分析,我们发现,当时先民的经营活动已经有明确的分工,其手工生产已经分出纺织、制陶和琢玉等门类,甚至还有酿酒,而且其工艺都达到一定的先进水平。在三四千年前的吴淞江流域的先民们竟然已经能够制作出精美的漆器了!总的来说,吴淞江流域的良渚文化时期的玉器形状和纹饰都是形式多样,工艺先进的。上面,笔者简要叙述了吴淞江流域远古文化中先进的手工业。......
2023-11-18

工业纯铜有普通纯铜、磷脱氧纯铜和无氧纯铜之分,它们主要是用来制造高导电性和导热性的零件的。这对原料、熔炼装置和熔炼工艺提出了严格的要求。为保证高纯无氧铜质量,有时需要经过多次脱氧才能满足要求,熔炼时还要严格控制好每个环节。表4-21列举了一些工业纯铜的感应电炉熔炼技术条件及操作顺序。......
2023-06-22

“十二五”陕西省工业节能发展思路、目标、重点及对策一、“十一五”期间陕西工业能耗指标完成情况在陕西省工业经济连续保持两位数增长的情况下,工业单位增加值能耗呈逐年下降态势。“十一五”前四年累计下降47.8%。“十一五”以来,省级财政共安排1.5亿元节能专项资金支持十大重点节能工程项目200余个,其中工业节能项目占90%以上,形成节能量280万吨标准煤。......
2023-11-30

NMMO水溶液的熔点会随溶剂浓度的提高而升高,溶解的工艺温度必须高于溶液的熔点。不能采用过高的温度和NMMO分解温度相关,实验表明,当温度超过130℃时,NMMO的分解反应明显增加。实验表明,NMMO水溶液在120℃时,便出现明显的变色反应,溶剂的变色是由于溶剂分解反应产生了带色基团,在生产中它将直接影响所生产纤维的颜色。......
2023-06-25

电子产品是以电能为工作基础,与电子信息技术有关的产品。研究电子整机产品的制造过程,材料、设备、方法、操作者这几个要素是电子工艺技术的基本重点。电子产品工艺技术、产品质量和生产效率的提高,主要依赖于生产设备技术水平和生产手段的提高。......
2023-06-20

渭南市“十二五”工业发展研究一、渭南工业发展现状“十一五”以来,市委、市政府大力实施“工业强市”战略,着力推进新型工业化进程,加快项目建设、环境建设和工业园区建设步伐,促进了工业生产持续快速增长,工业结构进一步优化,工业经济运行质量和效益明显提高,在市域经济发展中的主导作用明显增强,工业已成为拉动渭南市经济持续快速增长的主导力量。......
2023-11-30

由于水和NMMO的电负性不同,NMMO具有更强的与纤维素羟基形成氢键的能力,因此,当NMMO水溶液的浓度发生变化时,会对溶胀过程产生明显的影响。因此,通常认为要破坏纤维素大分子间氢键的NMMO溶液的浓度必须高于72%。许虎[2]等同样用溶胀后的浆粕经离心脱水后,测定浆粕质量的方法研究了在74%、76%和78%NMMO三种浓度下,浓度对溶胀性能的影响。结果发现,78%浓度的NMMO的溶胀性能明显的优于前两者。......
2023-06-25
相关推荐