政治组李红学习目标1.识记我国分配制度的内容;理解按劳分配的内容、必要性,生产要素按贡献参与分配的意义;区分现实生活中不同的分配方式,分析个人家庭收入的来源。因而在按劳分配中不能提“不劳不得”。教师要进行点拨式教学,帮助学生在教师所提问题基础上进一步质疑,发现并提出问题。让学生彻底明白各种分配方式,特别是对按劳分配、按劳动成果分配和按生产要素分配三者的区分。......
2023-07-31
化学组 谭冬梅
学习目标
1.学会物质的量在化学方程式计算中的应用。
重点难点
1.物质的量在化学方程式计算中的应用。
2.归纳总结物质的量用于化学方程式计算的基本步骤。
学习探究
1.物质的量在化学方程式计算中的应用
问题1:请对化学反应2Na+2H2O=2NaOH+H2↑给出至少5种不同的读法。
【思维点拨】可从定性和定量两个方面思考。
【设计理由】让学生从化学方程式不同读法中,理解化学方程式可以表达不同的意义,为物质的量用于方程式的计算做好铺垫。
【使用说明】引导学生从定性和定量两个方面思考回答教师提出的问题,可以采用抢答的方式让同学们读出此方程式的不同读法,让学生初步体会物质的量在化学方程式中的意义。
问题2:以化学反应2Na+2H2O=2NaOH+H2↑为例,寻找并推导化学方程式中各物质的化学计量数之比与粒子数之比、物质的量之比、相同条件下各气体体积之比的关系。
【设计理由】根据化学方程式表示的意义,让学生深刻理解化学方程式中物质的质量、物质的量与气体的体积之间的关系,让学生讨论推导出:化学计量数之比等于各物质的粒子数之比,也等于物质的物质的量之比,也等于相同条件下各气体物质的体积之比。突破了教学中的一个难点,也让学生寻找到了化学方程式计算的依据。
【使用说明】小组讨论完成后,代表小组上台展示交流。
2.物质的量应用于化学方程式的计算过程中需注意的问题
问题3:通过自学完成教材第52页的例题,思考根据化学方程式计算时,已知物理量与被求的物理量是否必须一致?
【设计理由】让学生自学完成教材的例题,目的在于让学生理解根据化学方程式计算时,已知物理量与被求的物理量不一定一致。为完成教学目标1迈出坚实的一步。
【使用说明】学生独立完成,老师巡视点拨。
问题4:请参照教材第52页例题中的书写格式,完成下列题目:用锌与盐酸反应制得标准状况下的H24.48L,需Zn的质量是多少?需2mol/L盐酸的体积是多少?若反应前后溶液的体积变化忽略不计,求生成ZnCl2的物质的量浓度为多少?反应中转移电子多少摩?
【设计理由】让学生模仿第52页例题中的书写格式完成此题,目的在于让学生悟出:物质的量与物质的量相比、质量与物质的量相比、体积与物质的量相比、质量与体积相比的各种情况,在教师的引导下归纳总结出化学方程式的计算列关系式的关键点:单位上下相同,左右相当。初步学会物质的量在化学方程式计算中的应用和初步学习化学反应中转移电子物质的量的计算。
【使用说明】实物投影学生课堂练习完成情况并评价、点拨。PPT投影规范解题格式,引导学生归纳总结物质的量用于化学方程式计算的基本步骤。
【思维拓展】将5.4g Al放入50mL 2mol/L的NaOH溶液中,反应完毕生成的H2在标准状况下的体积是多少?
【设计理由】设计此思维拓展题,目的是开阔学生的视野,让学生了解当已知两种反应物用量时,需要首先判断哪一个反应物过量,然后根据不足量的反应物求解。
【使用说明】此思维拓展题有一定的难度,不同学校可以根据学生的实际情况进行删减。
达株检测
1.一块表面已被氧化为Na2O的钠块10.8g,将其投入100 g水中,产生H20.2g,则被氧化的钠是( )。
A.9.2g B.10.6g C.6.2g D.4.6g
2.取两份等量的铝粉,分别与足量的盐酸、浓氢氧化钠溶液反应,在相同状态下产生的气体体积之比是( )。
A.1∶1 B.1∶2 C.1∶3 D.3∶2
3.医疗上颇为流行的“理疗特效热”,就是利用铁缓慢氧化放出均匀、稳定的热,使患者患处保持温热状态。若1mol铁粉完全氧化成氧化铁,需消耗氧气的质量为( )。
A.21g B.32g C.24g D.16g
*4.取18.4g铝锌合金溶于足量硫酸中,完全反应后收集到(标准状况)氢气11.2L,则由铝和锌分别产生的氢气的体积比为( )。
A.2∶3 B.3∶2 C.1∶3 D.3∶1
5.将2.3g金属钠放入100g水中,完全反应后溶液的质量分数为( )。
A.100% B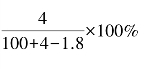
C![]() D
D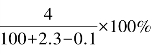
*6.将部分氧化的金属钠(假设氧化产物只有Na2O2)投入盛满水且倒置在水槽内的容器中,此时在容器中可收集到448mL气体(假定各步反应完全,并且产生的所有气体全部被收集到容器中,体积都是在标准状况下测得),以电火花引燃容器里的气体,最终剩余112mL氢气。求该钠块中未被氧化的钠及Na2O2的物质的量。
【设计理由】达标检测设计让学生初步体会到用物质的量计算比用质量计算更方便,试题难度由浅到深,在层层深入中完成目标1和目标2的学习,在解题过程中逐步掌握物质的量用于化学方程式计算的基本步骤。
【使用说明】根据学生实际情况选择使用,请酌情删减或增加。物质的量在化学方程式中的计算是第一章“物质的量”的相关计算的延续、深化,物质的量是化学计算的工具,化学计算贯穿于高中化学教学始终,化学计算教学应特别注意循序渐进、逐步深入,教师心中要有一个长远的教学计划。同时在化学计算教学中,教师要有目的、有针对性地培养学生的思维能力。应当巧妙地设置能启发学生思考的问题,从而最大限度地调动学生思维的积极性。创造条件鼓励学生积极思索,勇于探索。对在解决某一问题上有独特见解的学生要及时予以表扬和鼓励。以调动学生发现、捕捉规律,由此促使学生的思维由表象到本质向纵深发展,从而促进学生化学学科核心素养体系的形成。
有关天高地阔,凤举鸾翔 重庆市凤鸣山中学基于核心素养的课程改革探索与实践的文章

政治组李红学习目标1.识记我国分配制度的内容;理解按劳分配的内容、必要性,生产要素按贡献参与分配的意义;区分现实生活中不同的分配方式,分析个人家庭收入的来源。因而在按劳分配中不能提“不劳不得”。教师要进行点拨式教学,帮助学生在教师所提问题基础上进一步质疑,发现并提出问题。让学生彻底明白各种分配方式,特别是对按劳分配、按劳动成果分配和按生产要素分配三者的区分。......
2023-07-31

数学组王鹏飞学习目标1.(1)掌握任意角的正弦、余弦、正切的定义;(2)掌握正弦、余弦、正切函数的函数值的求解;(3)正确理解三角函数是以角为自变量的函数.2.在任意角三角函数概念的形成过程中,提高分析、探究、解决问题的能力,培养学生的直观想象能力,体会函数思想,培养学生抽象思维能力,体会数形结合思想.3.(1)使学生认识到事物之间是有联系的,三角函数就是角度(自变量)与比值(函数值)的一种联系......
2023-07-31

毕业设计课程的指导过程是教学相长的过程,是教师检验自身教学效果、改进教学方法、提高教学质量的绝好机会,更是对教学效果的一次全面反馈。可邀请理论水平高、实际经验丰富的专业技术人员担任毕业设计指导工作,可以促使设计和实际生产科研更紧密地结合。学生应及时提交毕业设计所规定的材料。学生应在导师的指导下,独立完成调研报告、流行趋势分析、设计及制作等过程,并及时提交毕业设计和相关材料。......
2023-06-22

图形设计的概念图形一词在英文中称为“Graphic”,源于拉丁文“Graphicus”和希腊文“Graphickos”。←(左)罗纳德设计的“和平”海报,小女孩的负形是各种动物组成的,体现人对自然的敬畏之心。↓(下)罗纳德设计的“和平”海报,孩子手牵手的负形正是一只鸽子,体现出人与自然之间和平共存的相处之道。→(右页)U.G.Sato设计,动物与人类共存。......
2024-01-25

物理组聂祜川学习目标1.理解和掌握动量、冲量的概念,强调动量、冲量的矢量性,并能正确计算一维空间内物体动量的变化。问题3:如何从牛顿第二定律入手推导动量定理?牛顿第二定律和动量定理本质上一样,只是在不同形式下的表现,这个问题可以让学生更加深刻地理解动量定理。问题4:动量定理反映哪两个量之间的关系?......
2023-07-31

复习课常用概念图、思维导图教学策略等。思维导图辅助高中生物学复习课教学有哪些优势呢?在高中生物学复习课中,教师引导学生综合运用文字、色彩和图形等绘制思维导图,将放射性思考的内容图式化,能提高学习自主性。学生共同制作思维导图,在体验中总结知识点及其联系,能提高学习兴趣。最终思维导图呈现为树状层级结构。......
2023-11-23

语文组冉静学习目标1.深入领会叙事性文体的特征,学会于事件中、细微处把握人物性格特点,体会作者对母亲的深厚感情。感受母亲深细而严格的教育及其深远的影响。——彭红《好人胡适》引入材料:胡适的《先母行述》和《奔丧到家》中的语句。进一步感受胡适对母亲真挚而深沉的情感。生活是作文的源泉。达株检测我的母亲母亲生在农家,勤俭诚实。......
2023-07-31

化学组谭俊秋学习目标1.了解有机合成的基本概念和物质合成过程的基本方法。问题6:从有机合成中你学到了哪些知识?学生通过反思总结本节课的学习内容,掌握有机合成的目的和方法,进一步实现目标1和2,同时培养学生的归纳总结能力,以及培养学生科学学习的核心素养和思维品质。......
2023-07-31
相关推荐