燃烧化学反应最重要的应用是,燃烧气体平衡构成和绝热火焰温度的计算。在实际燃烧反应中,几乎没有燃料与氧化剂直接反应生成燃烧生成物的情况。2分子反应是2个分子的反应,3分子反应是3个分子的反应。这称为化学平衡。......
2025-09-29
在成分复杂、基质很脏的情况下,被测分子往往会受到干扰而无法被准确地测定。延长被测分子在反相柱中的保留时间可以降低被干扰的概率。要延长分子的保留时间,特别是极性分子在反相柱中的保留时间,使用离子对的移动相是一个非常好的选择。
当被测分子是极性分子或离子时,可以在移动相中加入相反极性的离子,与被测离子在移动相中形成中性的离子对,从而可以在反相柱中延长保留时间,降低被干扰的概率。
如果被测分子是负极性的,可以在移动相中加入强碱性的正离子如季铵盐、叔铵盐等。常用的正离子有四甲基季铵盐、四乙基季铵盐、四丙基季铵盐等(图1-21)。一般加入碳原子数越多的季铵盐,就会得到越长的保留时间。但加入大分子的季铵盐对色谱仪及反相柱都有一定的损害。所以只要能达到分离的目的,应尽可能用相对分子质量较小的季铵盐做离子对。相反,假如被测分子是带正电的分子或离子,那么在移动相中就要加入强酸性的负离子,如磺酸盐等。常用的负离子有带4~10个甲基(丁到癸)的磺酸盐(图1-22)。同样,加入碳原子数越多的磺酸盐,保留时间就越长。但加入相对分子质量大的磺酸盐对仪器及反相柱都会有一定的损害,所以只要能达到目的,应尽量用相对分子质量小的磺酸盐来做离子对试剂加入移动相。
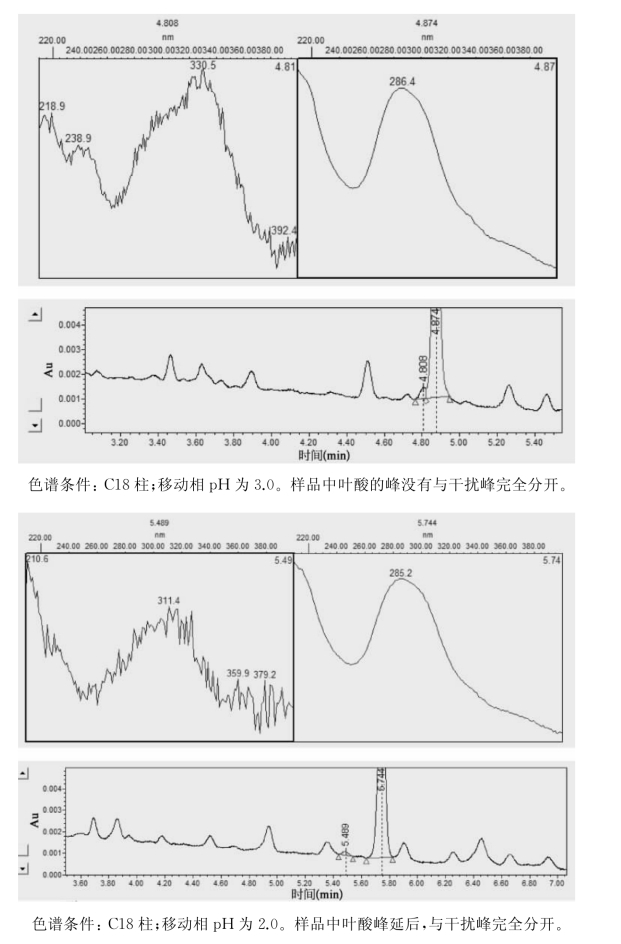
图1-20 移动相pH对叶酸测试的影响
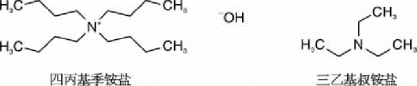
图1-21 可用作离子对的正离子
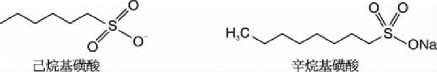
图1-22 可用作离子对的负离子
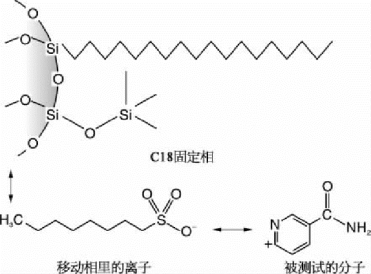
图1-23 离子对在色谱中的作用
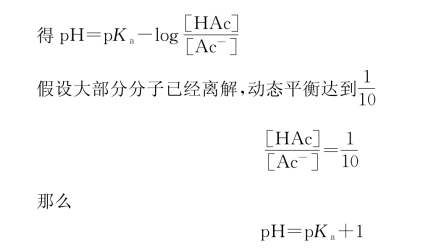
另外,含有离子对的移动相的p H 也是一个重要的参数。加入到移动相中的离子对的离子都是强酸性或强碱性的,在一般的p H 条件下(p H 1~7)极性的强弱不会有太大的变化,但是移动相的p H 对被测分子的极性可能会有很大的影响。比如,要用反相柱和含有四丙基季铵离子的移动相来测试醋酸和甲酸,移动相的p H 大概应在什么范围内?
根据公式:

 (https://www.chuimin.cn)
(https://www.chuimin.cn)
已知醋酸的p K a是4.76,假如要让离子对有效地工作,大部分的醋酸分子应处于离解状态,p H 应不小于p K a+1=5.76。所以要把移动相的p H 调节至不小于5.76。
已知甲酸的p K a是3.75,假如要用离子对来测试甲酸,那么移动相的p H 就应调节至不小于4.75。
反之,测碱性化合物时

这里B是碱分子,BH+是质子化的碱离子。
同样假设大部分碱分子被质子化了,动态平衡达到
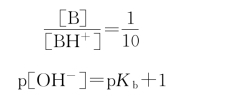
另因为p H=14-p OH
所以移动相的p H=14-p K b-1
因为14-p K b=p K a,所以也可以表达成
![]()
例如已知苯胺的p K b是9.13,假如用六甲基磺酸作为离子对,那么移动相的p H 应该是不大于14-9.13-1=3.87。
或也可表达为p H=p K a-1=(14-9.13)-1=3.87。
对于双极性分子(如氨基酸等),用离子对时,p H 的调节应根据分子的等电点来定。例如,半胱氨酸的等电点是5.05,也就是说在p H 为5.05时,半胱氨酸是中性、不带电的。但假如降低p H,整个分子就带正电;升高p H,分子就会显负电性。若要用烷基磺酸盐做离子对试剂,那么p H 就要调节至5.05-1=4.05以下;若要用季铵盐做离子对试剂,那么p H 要调节至5.05+1=6.05以上。
相关文章

燃烧化学反应最重要的应用是,燃烧气体平衡构成和绝热火焰温度的计算。在实际燃烧反应中,几乎没有燃料与氧化剂直接反应生成燃烧生成物的情况。2分子反应是2个分子的反应,3分子反应是3个分子的反应。这称为化学平衡。......
2025-09-29

一般来说,粒径在1~100nm之间的粒子称为纳米粒子。PVD法是在惰性气体中加热蒸发原材料,使材料汽化或形成等离子体,然后经冷却得到纳米粉末。其中,Nan-oxTMS2631P纳米Al2O3-13TiO2和武汉地大YSZ纳米团聚体粉末性能参见第4章的表4-28。......
2025-09-29

与此相比,煤油、四氧化二氮、硝酸等可在常温下以液体状态长时间储藏的燃料称为可储藏性推进剂。某种组合可以自燃并持续燃烧反应,把这种组合称为自燃性推进剂。......
2025-09-29

固体(态)继电器是采用固体半导体元件组装而成的一种无触点开关。但固体继电器也有不足之处,如漏电流大、接触电压大、触点单一、耐温及过载能力差等。现以JGC-3F型固体继电器为例,其电气参数见表2-3。图2-5和图2-5的结构基本相同,只是元件参数有所不同;图2-5为SSR型固体继电器与外界的接线图。当输入端A、B无电压输入时,运算放大器A的输出脉冲不能送到双向晶闸管V的控制极,V截止,负载脱离电源。......
2025-09-29

位于葡萄糖环2、3、6位置上的三个碳原子都与羟基相连,与碳2、碳3相连的是仲羟基,与碳6相连的则是伯羟基。伯、仲羟基具有不同的化学反应能力。黏胶纤维的中间体、醋酯纤维、硝化纤维都是纤维素通过特定的化学反应获得的纤维素的衍生物,而Lyocell纤维的抗原纤化处理则是交联剂与纤维素上的羟基发生化学反应的结果。......
2025-09-29

研究提出的实体坝身与透水结构坝头组合的新型丁坝结构型式,已成功应用于与长江中游河型、水沙条件、河床组成及河道边界基本一致的东流水道航道整治工程——老虎滩鱼骨坝工程中。......
2025-09-29

聚吡咯材料具有较多的应用,比如,利用聚吡咯的吸湿性能,可以捕获环境中的湿气,且随着湿度的增强,聚吡咯的离子导通作用占据主导作用。改变外电压,可以调控聚吡咯的掺杂、去掺杂状态以及掺杂水平。以上结果表明,聚吡咯可以作为新的能量转化体系的功能化材料。本节主要基于一维聚吡咯纳米线制备了一种独特的利用单价阳离子迁移实现的纳米线发电机。......
2025-09-29

电子鼻是一种气味扫描仪,是20世纪90年代发展起来的快速检测食品品质的新型仪器。运用电子鼻技术检测稻米散发的气味,能够快速、准确地判断稻米是否发生霉变。梁爱华等采用电子鼻技术分别检测3种不同品质的方便米饭,通过对主要成分的分析和气味指纹对比,结果表明,电子鼻能够识别不同香味的方便米饭。另外,在电子鼻分析中,特征提取、模式识别方法的完善,是否应配置富集装置进行样品试验,也有待进一步确证。......
2025-09-29
相关推荐