桩基随着土层的压缩模量变化也会相应地导致沉降。冯忠居[15]分析了桩及桩周土浸水期间的沉降变化规律。孙金柱[18]通过在桩-土相互作用下土的弹性模量、桩长和桩径这3个因素对桩基础沉降影响进行了分析研究。直至目前阶段单桩沉降与群桩沉降之间关系的研究还不成熟。蒋媛[20]提出利用Mindlin位移解计算桩桩相互作用,以群桩中桩基的平均荷载控制群桩沉降计算时的土体弹性模量取值的单桩推算群桩的方法。......
2023-08-23
可燃混合气在某一温度下自燃着火的现象称为自燃(或自发着火、自着火),与此相反,以某种外部手段向部分混合气提供能量使混合气着火的方式称为点火(或强制点火)。汽油机利用火花塞点火开始燃烧,柴油机利用自燃开始燃烧。
1.着火
可燃混合气能着火,其燃料的活性化学物质起着非常重要的作用。为了自发进行燃烧反应,必须积蓄和供给充分浓度的活性化学物种。为此所提供的最低温度称为燃点。燃点随燃料和氧化剂的种类、当量比、容器的形状或大小等的不同而会发生变化。
着火机制有热着火理论和链锁着火理论。热着火理论可以利用燃点进行推导。
(1)热着火理论 热着火理论把燃烧反应以一个总括反应进行分析,通过反应的产热速度等于或大于向周围的热损失速度,决定是否可以着火。如果火花塞的电极离燃烧室壁越近,其低温起动性能越不良。这是因为火花点火的混合气发热速度低于通过周围金属的散热速度所致。发热是反应速度相关问题,由燃料和氧化剂的组合、当量比、温度和压力等决定。热损失是热传递相关问题,由周围温度差、热传递系数等决定。
图4-29a显示了火花塞点火热着火理论的模型。假设火花塞间隙体积为由电极包围的容器。
此时,容器(间隙)内可燃混合气的反应热产生速度 为根据阿伦尼乌斯反应定律可以表示为
为根据阿伦尼乌斯反应定律可以表示为
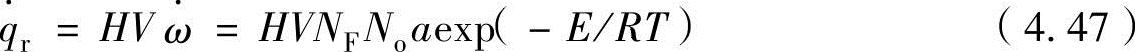
式中,H为通过反应的混合气摩尔发热量;V为容器容积;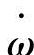 为反应速度;NF、No分别为燃料和氧化剂的浓度;a为周期因数;E为活性化能量;R为一般气体常数;T为混合气的温度。
为反应速度;NF、No分别为燃料和氧化剂的浓度;a为周期因数;E为活性化能量;R为一般气体常数;T为混合气的温度。
设定容器壁面的温度为Tw,通过容器壁面的热损失速度 的计算公式为
的计算公式为

式中,h为热传递系数;A为容器的表面积。
热产生速度和热损失速度之间关系如图4-29b所示。热产生速度随混合气温度T的增加以指数函数增加,压力以p1、p2、p3逐步上升时,曲线向上移动。热损失速度与混合气温度和壁面温度之差成正比例,与压力无关显示为一条直线。此直线在压力为p2时在点c进行交叉。自燃的条件为必须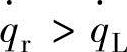 。因此,压力大于p2的p3状态,燃烧温度会急剧上升结果会达到爆发的温度;压力小于p2的p1状态,在超出点a、b的位置上发生着火。
。因此,压力大于p2的p3状态,燃烧温度会急剧上升结果会达到爆发的温度;压力小于p2的p1状态,在超出点a、b的位置上发生着火。
自燃的条件为点c的温度即Tc为两条线相交叉的位置。在此条件下,因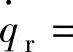
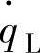 ,如下公式成立:
,如下公式成立:
HVNFNoaexp(-E/RT)=hA(T-Tw)
在着火初期,因燃料与氧化剂的浓度大体上不会发生变化,可以看成为常数,并对上式以温度T进行微分,可以推导出下式。
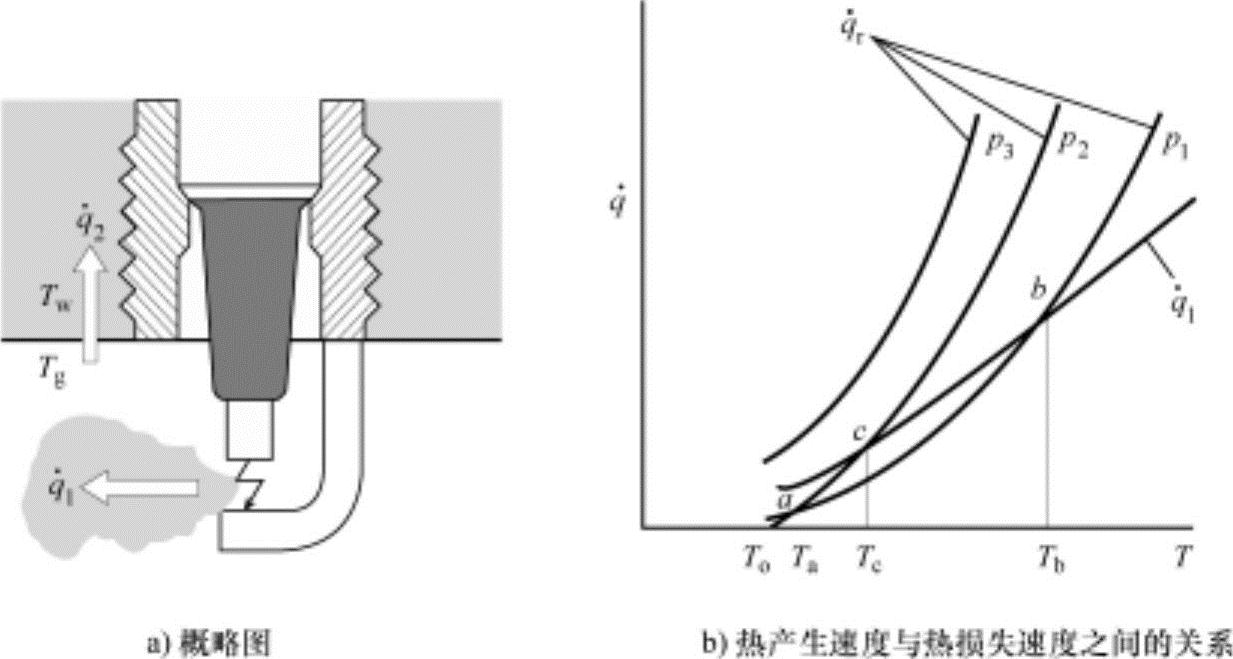
图4-29 热着火理论模型
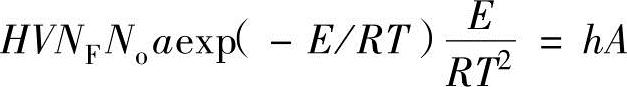
根据上述两个公式可以推导出

在上述二次方程式的两个根中,大的根温度相当大,不符合实际情况,因此小的根对应于燃点。因此,

通常,4R/E=(0.1~0.3)×10-3,即使设定壁面温度为Tw=1000K,4RTw/E小于1,因此展开上式获得
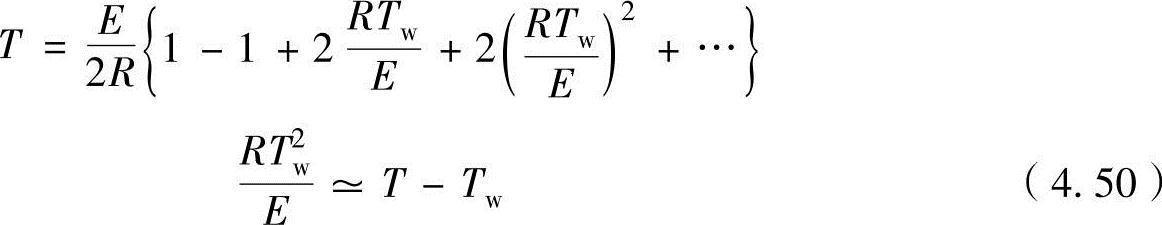
比较式(4.49)和式(4.50),可以看出Tw T。举例说明,设定E=179kJ/mol、Tw=1000K,可以得出T-Tw=49K,可以看出其差异仅为5%左右,故可把着火容器的温度近似看成周围的温度。因此,对静态燃烧器进行加热,当容器内部混合气着火时,可以看成容器内避免的温度就是着火温度。
T。举例说明,设定E=179kJ/mol、Tw=1000K,可以得出T-Tw=49K,可以看出其差异仅为5%左右,故可把着火容器的温度近似看成周围的温度。因此,对静态燃烧器进行加热,当容器内部混合气着火时,可以看成容器内避免的温度就是着火温度。
(2)链着火理论 链着火理论是活性化学物质(又称为活性基、链源、自由基)的生成速度比消灭速度大时发生着火的原理。
图4-30所示为氢气-氧气理论混合气自发着火后急剧燃烧开始的界限。当压力一定时,与压力所对应的燃点仅为一个,但当温度一定时,随压力的变化,可能发生着火也可能不发生着火,会出现第一、第二、第三燃烧界限。这时通过热着火理论无法进行说明,但可以利用链着火理论进行说明。
①第一燃烧界限:这是支链反应和通过容器的链终止反应所致的,扩散速度的降低促进着火。在图中点A领域,因压力低,活性化学物质之间的碰撞频率低,也不能进行充分的碰撞,不仅活性基的生成速度低,连生成的活性基也与容器壁面接触失去其活性并消失。但是,会产生不能称为燃烧的缓慢的氧化反应,一旦经过长时间,容器内的成分会发生变化。
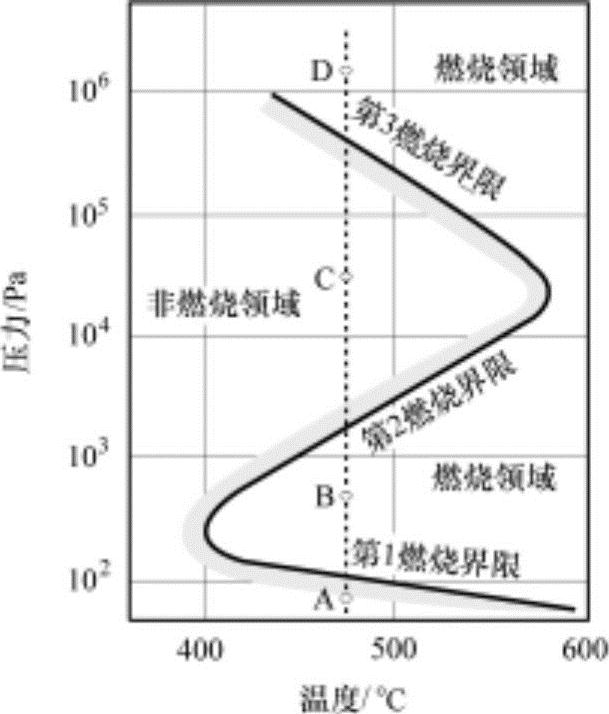
图4-30 氢气-氧气理论混合气的燃烧界限
②第二燃烧界限:这是支链反应和气状终止反应中链终止第三成分M所致。在点B领域中,压力较大,活性基之间高频率发生碰撞,从而发生支链反应,在容器壁面上的活性基失活率减小,结果活性基急速增加,因此发生燃烧反应。
③第三燃烧界限:不是链机制,可能因反应速度快,会发生自加热,因而热着火性能包含在内。在点C领域中,压力非常大,因而化学物质之间的碰撞频率更高,在此领域与在点B领域几乎没有的第三成分的碰撞增加,活性基的失活速度超过增加速度,因此不能发生燃烧反应。
超过第三燃烧界限,在点D领域中,压力更大,因此化学物质之间的碰撞更加强大,在点C领域中抑制活性基增长的HO2,在此领域与燃料中的H2发生反应,使化学反应重新活泼起来,因而发生热着火燃烧反应。
第三界限对应于热爆发临界压力p0,在临界压力以上发生反应时,因温度上升会发生更加旺盛的燃烧反应。
2.点火
预混合气温度不会达到自燃点以上发生着火,而用电火花塞、炙热的高温物体(预热塞)等强制进行点火。这是向部分混合气提供能量发生着火的方式,点火条件在于是否形成能进行火焰传播的火焰内核。
(1)火花点火 汽油具有良好的蒸发特性和着火特性,在很低的温度下也能容易自燃。因此,汽油机为了防止自燃不能过分提高压缩比,而是通过电火花强制进行点火。
电火花能量过大或过小也会成为问题。如果点火能量过大,会发生异常燃烧(爆炸:冲击波和燃烧现象重叠的现象),如果点火能量过小,因对火焰的电极冷却作用增加,在火花塞间隙中生成的活性基的增速低于消失速度,因而不能形成火焰内核,进而不能进行火焰传播。把能进行火焰传播的临界能量称为最小点火能量。最小点火能量与燃料和氧化剂的种类、混合气的混合比、压力、温度、混合气的流动状态、电极间隙、电极形状等多种要素相关。
最小点火能量不仅随混合气状态的变化而改变,还会因电极形状的不同而改变。图4-31所示为天然气与空气的理论混合比状态电极间隙与最小点火能量之间的关系。棒型火花塞电极的电极间隙越小,最小点火能量就会越低,在某一间隙时达到最小点火能量。此时如果减小电极间隙,相反最小点火能量开始增加,这是因为对火焰内核的电极冷却作用增大所致。此时增加电极点火能量,即使间隙小也可以达到着火能量。对于附加法兰的电极来说,当电极间隙达到dt,min以下时,因通过法兰的热损失冷却效果过大,即使增大电极点火能量也不能达到着火能量。
多种碳氢化合物燃料在大气压、室温条件下的最小点火能量与当量比之间的关系如图4-32所示。最小点火能量是像甲烷(CH4)等分子量较小的燃料在比理论混合比稀薄侧,像庚烷(C6H14)等分子量较大的燃料在浓混合比侧,这是因为燃料分子和氧气分子之间的扩散速度差所致。碳氢化合物燃料的最小点火能量的最小值为在任何状态下为0.2~0.3mJ,随燃料的成分不同有所差异,氢气(H2)的最小点火能量远低于这些燃料,约为1/10。通常,混合气的压力越低、温度越低、流速越高或稀薄气体的比例越高,最小点火能量就越大。
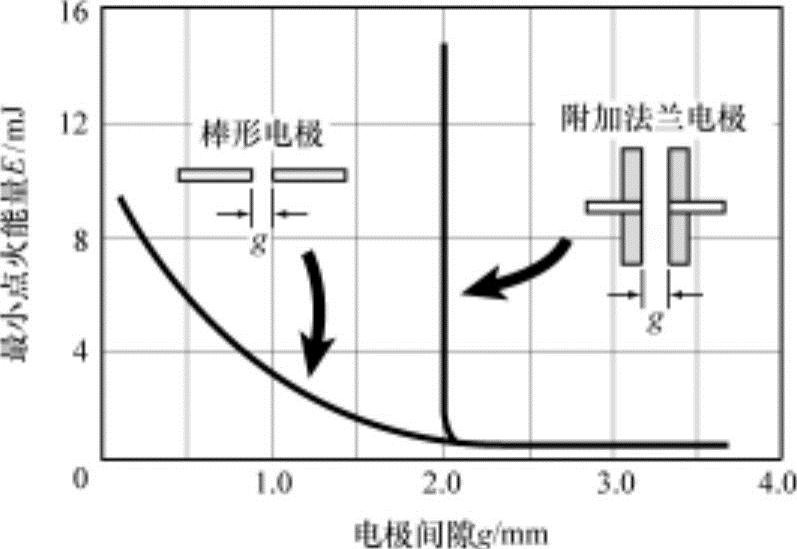
图4-31 电极间隙与最小点火能量
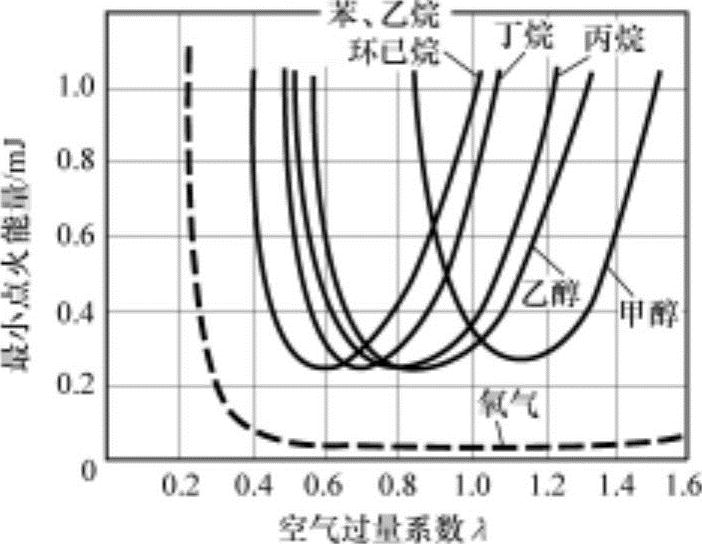
图4-32 各种燃料的最小点火能量
(2)通过高温物体的点火 柴油机、城市天然气简易点火器等利用镍铬合金加热线等高温物体点燃混合气。此时的点火是,在灼热表面附近的混合气在高温作用下达到自燃温度以上时开始燃烧反应。此时虽然加热表面的温度最高,但壁面上的活性化学物种会失活,因此在稍微离开的表面部位会发生着火。因此,高温物体表面温度通常远高于混合气的气体状态自燃温度,着火源越小、混合气的压力和温度越低、着火源与混合气之间的相对速度越大、混合气中的湍流越强,表面温度会越高。对此,利用催化剂促进反应,就可以使表面温度低于自燃温度。
有关内燃机学的文章

桩基随着土层的压缩模量变化也会相应地导致沉降。冯忠居[15]分析了桩及桩周土浸水期间的沉降变化规律。孙金柱[18]通过在桩-土相互作用下土的弹性模量、桩长和桩径这3个因素对桩基础沉降影响进行了分析研究。直至目前阶段单桩沉降与群桩沉降之间关系的研究还不成熟。蒋媛[20]提出利用Mindlin位移解计算桩桩相互作用,以群桩中桩基的平均荷载控制群桩沉降计算时的土体弹性模量取值的单桩推算群桩的方法。......
2023-08-23

表面物质在摩擦过程中不断损失的现象称为磨损。根据黏着程度的不同,黏着磨损可分为轻微磨损、涂抹、擦伤、胶合和咬死。这种磨粒的机械作用在很大程度上与磨粒的硬度、大小和形状以及载荷作用下磨粒与被磨损面的机械性能有关。齿轮和滚动轴承的主要磨损形式就是表面疲劳磨损。......
2023-06-16

不同地点、不同时间进行的暴露试验研究表明,环境温度、湿度与SO2共同对锌腐蚀起作用,SO2污染是锌腐蚀的主要因素。工业城市大气以SO2污染为主;沿海地区海盐粒子是主要污染因素;森林和热带雨林地区空气洁净,锌腐蚀属于潮湿的大气腐蚀。对试验区域主要污染物SO2的监测结果表面,SO2浓度与材料腐蚀率成正比,地表SO2浓度较大,9m高度处浓度最小。......
2023-06-23

(一)阻燃涤纶热裂解—气相色谱/质谱联用测试对未处理、经DOPO或DFR浸渍法阻燃整理的涤纶织物采用Py-GC/MS研究其在600℃热裂解的过程中产生的气相产物,结果见表2-11~表2-13。因此,结合热分析中阻燃涤纶残炭含量几乎不增加的现象,认为DOPO用于涤纶阻燃,主要通过气相机理起作用。据此分析,DFR的存在会促进涤纶按这一路径的降解,DFR对涤纶阻燃也包含凝聚相机理。......
2023-06-26

图6-27 铣刀前刀面的显微照片当铣削速度v=40m/min时,铣刀前刀面是月牙洼磨损形态,见图6-29a。总之,在低速铣削工件时,铣刀前刀面是月牙洼的磨损形态,以粘结磨损为主;随着铣削速度的提高,刀具前刀面的粘结磨损减轻,伴有磨粒磨损;当铣削速度的进一步提高时,刀具有微小的崩刃,磨粒磨损也在增大。......
2023-06-27

拔下点火线圈线束连接器,用万用表欧姆挡检测点火线圈各线圈的电阻值,其值应符合表2.2 的规定;如不符合,则必须更换点火线圈。图2.32丰田皇冠3.02JZ-GE 发动机点火系统电路表2.2点火线圈电阻值②点火控制器的检测。双缸同时点火时,高压电的分配有二极管分配和点火线圈分配两种形式。点火控制器中的两只功率晶体管分别控制一个初级绕组,两只功率晶体管由ECU 按点火顺序交替控制其导通与截止。......
2023-08-23

能够按时在火花塞电极间产生电火花的全部设备称为点火系统。如图4-96所示,现代发动机的电控点火系统通常由蓄电池、ECU、点火器、高压导线、点火线圈和火花塞等组成。如火花塞发出蓝白色火花表明点火正常;如火花塞不跳火,说明点火系统有故障;若火花微弱,说明火花塞两极间严重短路;若火花不在中央,说明火花塞积炭或油垢过多;若瓷体和缸盖之间跳火,说明绝缘瓷体漏电。......
2023-09-17

鉴于“大五”人格模型中一些维度在西方音乐心理学具有一些实证研究的基础,故本研究将依据文献梳理、逻辑推断,运用大五人格模型中的若干维度,形成本研究的假设体系。性格与音乐的互动研究,更是方兴未艾。......
2023-11-04
相关推荐