影响气体在金属中平衡溶解度的因素有温度、压力、金属蒸气压、气体与金属的作用性质、化合物气体。它们在金属中的溶解度服从上述规律,即与压力的平方根成正比,并随温度的升高而增大。类金属氧化物则随温度升高而分解,从而使气体在金属中的溶解度降低。......
2023-06-26
在一般情况下,氧能与金属形成氧化物,而溶解在某些金属中,但溶解度较低,一部分则作为氧化渣浮于金属液面而被排除。氧在熔化的银中的溶解度最高。
氢能溶解在大多数的金属中,在铝、镁及某些高熔点金属中,溶解度比较高;在铅、锌等低熔点金属中溶解度就比较低。
氮在许多金属中的溶解度都极低,在某些金属中则不溶解。因此,因内外多把这种惰性气体作为一种除气剂来清除金属液中的气体。
氯和其他卤族元素不溶于熔融金属中,所以氯也可用做铝及铝合金的除气剂。
惰性气体(氩、氦、氟利昂等)不溶于金属液中,故氩气能除去镁合金中溶解的气体。
气体溶解度是指在某温度时,金属在该气体压力为一个大气压作用下达到平衡情况下的数值。
1.铝及铝合金
铝及铝合金极容易吸氢,它们所吸收的气体中,85%以上是氢,其余为氧、氮及碳与氢的化合物。氢在铝中的溶解度可根据Ransley公式进行精确测定,用下式表示:
在固态铝中lgS=±0.652-2080/T+1/2lgpH2
在液态铝中lgS=1.356-2760/T+1/2lgpH2式中T——热力学温度(K);
pH2——氢气分压力(Pa);
S——氢的溶解度(cm3/100g)。
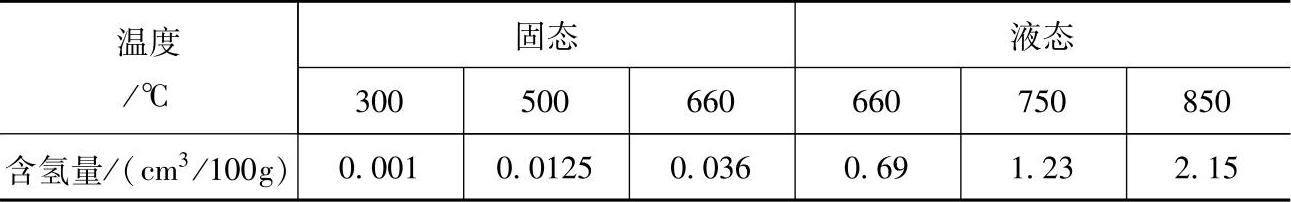
Ransley与Neufeld测得氢在纯铝中的溶解度见表1-3。
表1-3 氢在纯铝中的溶解度
氢在铝合金中的溶解度随合金化元素的增加而降低,具体要根据加入合金化元素本身溶解氢的能力是比基体金属强还是弱来决定。在纯铝中加铜或硅后都会使氢的溶解度降低,在其中加入铜后,氢的溶解度急剧减低;在铝及铝合金中加镁后,氢的溶解度反而急剧增大。
其他气体在铝中的溶解度一般都不明显,危害性不如氢那么严重,氢是铝及铝合金中危害性最严重的气体。铝液温度急剧下降到其凝固温度时,氢的溶解度也急剧减少,但仍会在铸件中形成气孔。
添加的合金元素若能使铝的表面膜更加致密(如加入铍),就可使氢的溶解度降低。这样可以减少吸气的量。
2.镁及镁合金
氢在固态及液态镁中的溶解度很高。在一个大气压下,在熔点650℃时,每100g镁可溶解20mm3(标准状态下)的氢,从650℃的熔化镁至液态时,可溶解26mm3的氢,达到900℃时,则可溶解30mm3的氢。
3.铜及铜合金
氢在铜中的溶解度相当大,1000℃的铜液中,氢的溶解度为5.73mm3/100g。在铜中加镍,氢的溶解度随镍添加量的增加而增大。含有二氧化硫的水蒸气也易溶解在铜中,而SO、CO2及N2则不溶于铜中。
4.镍
镍溶解氢气的能力也很强,在温度为1455℃时,氢在液态镍中的溶解度为39mm3/100g,再升温到1550℃就达到42mm3/100g,而在1455℃,氢在固态镍中的溶解度也达到17mm3/100g。
5.钛
氢在钛中的溶解度较小,Ti与H2之间的反应是放热反应,产物为TiH及TiH2,反应可逆。
6.铁与钢
氢在纯铁中的溶解度随着温度的升高而增大,但不明显;氮在铁液中的溶解度与氢相差不多。向铁中加入合金元素时,对氮的溶解度影响很大。氧以氧化铁的形式溶解在铁液中,达到饱和状态时,就在铁液面上形成氧化物膜,在熔化温度与一个大气压下且氧气相平衡的铁液中,氧化铁的溶解度为0.17%(质量分数),温度升高后,溶解度降低。
有关非铁合金铸造用熔剂和中间合金的文章

影响气体在金属中平衡溶解度的因素有温度、压力、金属蒸气压、气体与金属的作用性质、化合物气体。它们在金属中的溶解度服从上述规律,即与压力的平方根成正比,并随温度的升高而增大。类金属氧化物则随温度升高而分解,从而使气体在金属中的溶解度降低。......
2023-06-26

若在高温溶解的氢处于饱和状态,温度降低时,氢就会从金属液中析出。要了解氢气等气体从金属液中析出的速度和最终结果,必须弄清金属液析氢等气体的动力学过程。......
2023-06-26

化学吸附时金属与被吸附的气体间的结合力比物理吸附大得多。气体的扩散 被化学吸附在金属表面的气体,如能溶解在该金属中,它就会向此金属内部扩散。气体在金属中的溶解度一般较小,但也会使金属的体积发生变化,并伴随着吸热、放热现象发生。......
2023-06-26

SF6气体是目前镁工业中最广泛使用的保护气体。在进行镁熔炼保护时,通过将少量SF6气体和CO2气体及干燥空气充分混合以后覆盖在镁熔体表面进行保护。鉴于以上原因,SF6已经受到环境保护人员的严重关注。一些工厂及研究机构对SO2的保护作用做了深入的探索,应用结果表明,通过改进混气设备、增加安全装置并严格控制操作工艺,SO2可以用于镁熔体保护。一般认为SO2的保护机理是由于混合气体与镁熔体反应生成的多层复合保护膜而具有保护性。......
2023-06-22

非铁金属合金适合于仪器、仪表工业及在腐蚀性介质中工作的轻载荷齿轮,以及机械传动用蜗轮等。用作齿轮的非铁金属合金主要是铜合金。为节约贵重的铜合金,直径100~200mm青铜蜗轮的轮缘用青铜做成,轮毂用灰铸铁或钢制造。......
2023-06-29

前节所述的旋转除气的方法也属于吸附精炼的方法之一。镁比铝更容易和氮反应,生成Mg3N2夹杂物,因此对ZL301、ZL303、ZL305不希望用氮气精炼。工业用氩气瓶中含氧量较低,在0.005%~0.05%范围内,精炼温度允许提高到760℃。氩的密度为1.78g/cm3,高于氧的密度1.25g/cm3,通氩气精炼时,较重的氩气富集在铝熔池表面,能保护铝液,防止和炉气反应,故净化效果好。液态MgCl2有辅助精炼作用,当精炼温度低于715℃时,固态MgCl2则成为夹杂物进入熔渣中,因此精炼温度要求高于730℃。......
2023-06-22

表3-3-28 常用气体钎剂的种类和用途在炉中钎焊中可用作钎剂的气体主要是气态的无机卤化物,包括氯化氢、氟化氢、三氟化硼、三氯化硼和三氯化磷等气体。该气体钎剂也应添加到惰性气体中使用,并使体积分数控制在0.001%~0.1%的范围内。火焰钎焊时,可采用硼有机化合物的蒸气作为气体钎剂,如硼酸甲酯蒸气等。该蒸气在燃气中供给,并在火焰中与氧反应生成硼酐,从而起到钎剂的作用,可在高于900℃时钎焊碳钢、铜及铜合金等。......
2023-06-26
相关推荐