分析研究影响年径流量的因素,对年径流量的分析与计算具有重要的意义。这些因素主要从两方面影响年径流量,一方面通过流域蓄水变量ΔW影响年径流量的变化;另一方面,通过对气候因素的影响间接地对年径流量发生作用。所以,高程的增加对降水和蒸发的影响,一般情况下将使年径流量随高程的增加而增大。这些人类活动在改变年径流量的同时也改变了径流的年内分配。......
2025-09-29
各种纯金属的表面张力的大小,可根据金属原子体积大小及绝对熵这两个因素来判断。原子体积和绝对熵较大的金属,其表面张力较小,反之亦然。对同一种金属及合金而言,影响表面张力的因素有:温度、杂质及合金元素、结晶形状、熔剂。
1.温度的影响
物质的表面张力随温度的变化而变化。在一般情况下,金属液的温度升高、体积膨胀,原子间距拉长,削弱了其分子间的结合力,则其表面张力降低。这可用温度系数来表示:(dσ/dt)Mg=-0.34erg/(cm2·℃);(dσ/dt)Zn=-0.25erg/(cm2·℃);(dσ/dt)Al=-0.35erg/(cm2·℃)。在一定的温度范围内,许多物质的表面张力与温度呈线性变化,温度系数dσ/dt为负值,说明随着温度的升高,表面张力σ数值下降。图1-7所示为几种金属的表面张力与温度的关系。
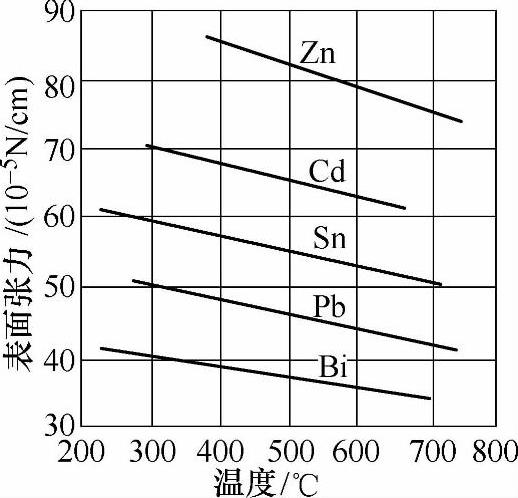
图1-7 几种金属的表面张力与温度的关系
在临界温度时,气、液两相无区别,表面张力等于零。许多物质的表面张力与温度有一定关系。
少数物质,如镉、铁、铜及其合金和若干硅酸盐的表面张力却随温度升高而增大。此种现象目前尚未获得应有的解释。例如:铜的表面张力在温度从1130℃升高到1250℃时,却增大6.29dyn/cm。
苯、二硫化碳、四氯化碳、乙醚、四羰基镍等物质的温度系数K约为2.1erg/℃。对于水、酒精及一些有机酸,K值不但小于2.1erg/℃,且随温度的变化而变化。
2.杂质及合金元素的影响
(1)微量元素的影响 在金属液中含有微量元素时,若该元素属活性物质,则此元素将富集于金属液的表面层,因吸附作用使金属液的表面张力σ降低;若该元素属非活性元素,则金属液的表面张力σ将增大。
原子体积较大的熔融金属属于活性物质。这样,当其聚积在金属液表面时,就使其表层的平均原子体积增大,因而降低了表面自由能,这是一个自发过程。如Al、Mg、Zn、Sn、Sb、Bi(它们的原子体积分别为11.40cm3/g原子、15.7cm3/g原子、17.1cm3/g原子、18.9cm3/g原子、19.5cm3/g原子、20.91cm3/g原子)等元素就是活性物质,而Cu、Fe(它们的原子体积分别是7.94cm3/g原子及8.2cm3/g原子)等就是非活性物质。活性物质能使表面张力σ急剧减小,非活性物质则使表面张力σ增大。
(2)加入元素熔点的影响 加入元素的熔点越高,其原子间的结合力越大,其表面张力也越大。
(3)夹杂物的影响 若金属液中的夹杂物与金属液分子之间吸引力大于金属本身分子间的吸引力,则金属液的表面张力σ增大;反之,则减小。(https://www.chuimin.cn)
3.结晶形状的影响
合金的结晶形状为球状、短柱状时,则会增大合金液的表面张力。
4.熔剂的影响
一些用表面活性元素(如RE等)配制的熔剂,通过物理吸附和增加反应层的厚度两方面的作用,可降低金属液/氧化膜的表面张力,并提高氧化膜表面的致密性。如用混合稀土RE配制的熔剂来熔炼ZMgAl8Zn,就能使其表面张力降低,使镁合金液形成正吸附,使RE在其表面富集并参与界面反应,在熔体和氧化膜之间形成一层富RE氧化物的致密的有保护作用的氧化膜,强力阻止Mg原子与O2接触的几率,有效地阻止了Mg原子的氧化,并阻止镁合金液的燃烧或爆炸。图1-8所示为RE表面富集的示意图。同时由于RE在氧化膜和熔体间的富集,会降低熔体/氧化膜间的表面张力。这是因为RE在镁合金熔体内发生正吸附,使镁熔体的表面张力降低,并使氧化膜处于低能量的状态,不易起皱和破裂。
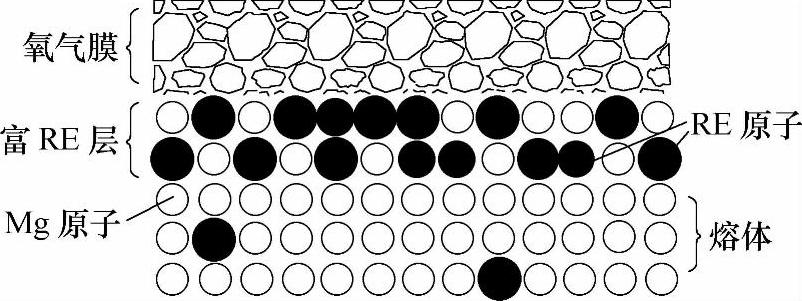
图1-8 RE表面富集示意图
由于RE参与界面反应会形成反应层,使熔体/反应层界面与氧化膜底面不在同一直线上,二者之间有一定的夹角,最终导致固/液界面张力方向发生变化,产生由氧化膜指向熔体内部的分压力F。根据界面反应润湿模型(图1-9)可得
F=σ1-scosθ (1-8)
RE的富集会增加反应层的厚度,使θ增大,根据式(1-8),θ增大,氧化膜指向熔体内部的分压力F也增大,这就可提高氧化膜与金属液之间的粘附能力,使氧化膜不容易破裂,从而增加了氧化膜的防氧化、防燃烧、防爆炸等的能力。
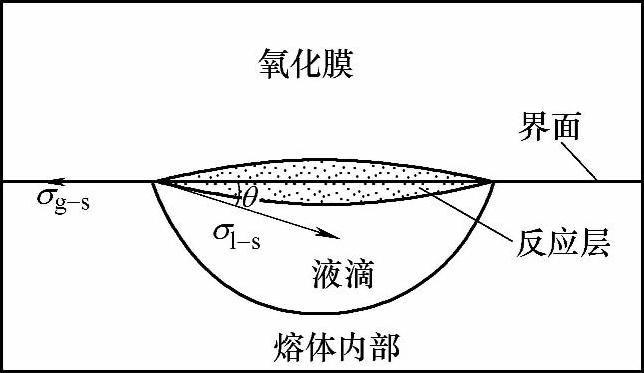
图1-9 界面反应润湿模型
相关文章

分析研究影响年径流量的因素,对年径流量的分析与计算具有重要的意义。这些因素主要从两方面影响年径流量,一方面通过流域蓄水变量ΔW影响年径流量的变化;另一方面,通过对气候因素的影响间接地对年径流量发生作用。所以,高程的增加对降水和蒸发的影响,一般情况下将使年径流量随高程的增加而增大。这些人类活动在改变年径流量的同时也改变了径流的年内分配。......
2025-09-29

图2.24活性药型罩锥角对活性射流头部速度的影响活性药型罩锥角不同时,活性射流速度分布及温度分布数值模拟结果如图2.25和图2.26所示。此外,从图2.25和图2.26中还可看出,活性药型罩锥角对活性射流成形形貌也有较大影响。其主要原因在于,活性药型罩锥角的增加可降低活性射流速度梯度,从而提高活性射流的凝聚性以及连续性。......
2025-09-29

影响数据质量的因素有很多,既有技术方面的因素,又有管理方面的因素。无论由哪个方面的因素造成的,其结果均表现为数据没有达到预期的质量指标[8]。图10-1数据的生命周期数据收集是指根据用户需求或者实际应用出发,收集相关数据。在数据收集阶段,引起数据质量问题发生的因素主要包括数据来源和数据录入。严格来说,数据备份阶段并不存在质量问题,它只是为数据使用提供一个安全和可靠的存储环境。......
2025-09-29

工艺焊接性是通过金属材料焊接性试验来实现,而使用焊接性则通过焊接工艺评定来实现。例如,钛金属在焊接过程中,400℃以上的区域都要用惰性气体保护,否则,该温度区域的钛金属氧化,力学性能变差,因此,焊接钛金属比焊接低碳钢要难得多。如钛金属用真空电子束焊接方法很容易获得高质量的焊缝,而用氩弧焊方法焊接,需要设计一套保护装置,在焊接过程中,将400℃以上的区域进行氩气保护,防止钛金属的氧化。......
2025-09-29

由杨氏方程可知,任何使三相表面张力发生变化,从而使接触角θ发生变化(减少)的因素都将影响钎料对母材的润湿性。从物理意义上说,如使σLV减小,意味着液体内部原子对表面原子的吸引力减弱,液体原子容易克服本身受到的引力趋向液体表面,使液体的表面积增大,钎料容易铺展。而σSV增大,说明固体的内部原子对表面原子的吸引力增大,表面原子处于高能态。......
2025-09-29

纤维素纺丝工艺的选择与纺丝液的黏度直接相关,而纺丝液的黏度又与诸多因素相关联,例如,溶液中的纤维素含量、纤维素的聚合度、纺丝液温度等都会影响纺丝液的黏度。低含量纤维素或低聚合度纤维素制成的纺丝液具有较低的黏度,它有利于纺丝,但经济性不佳。因此,人们总是希望在确保纺丝工艺顺利进行的同时,尽可能地提高纺丝液中纤维素的含量。......
2025-09-29

图4-1-39列出了影响激光切割质量的主要材料特性。激光模式及光束质量对切割质量的影响 激光模式决定了聚焦焦点的能量分布,对切割质量影响非常大。而多模激光的能量分布是不对称的,所以不同方向的切口宽度可能不均一,质量也可能不同。......
2025-09-29

气阀钢是在高温下使用的热强钢类,它对钢的冶金质量有较严格的要求。这将对气阀钢的高温强度、韧性和耐热腐蚀等性能产生显著的影响。硅是平衡钢中含氧量的主要脱氧元素。......
2025-09-29
相关推荐