所以,目前还不能对发酵进行全面控制,使其按人的意志进行目标产物的生物合成。但是,掌握发酵工艺条件对发酵过程的影响以及微生物代谢过程的变化规律,可以帮助人们有效地控制微生物生长和代谢产物的发酵生产,不断提高发酵水平。此外,通过发酵动力学研究,建立能定量描述发酵的过程的数学模型,并借助现代过程控制手段,为发酵生产的优化控制提供技术和条件支持。......
2023-11-18
一、生产前准备
(一)查找资料,了解卡介苗生产的基本知识
1.结核病
结核病是由结核分枝杆菌引起的人畜共患的慢性缓发的传染病。据WHO报道,目前全世界约有10亿结核菌感染者,每年还会有约800万新增病例产生。虽然结核病是可以治愈的疾病,但每年仍有300万人死于结核病。我国是世界上22个结核病高负担国家之一,我国三分之一左右的人口已感染了结核菌,受感染人数超过4亿。一些地区因艾滋病、吸毒等,合并结核病死亡率已经超过70%。结核病的特异性预防是接种卡介苗。
2.卡介苗
卡介苗(bacillus calmette guerin,BCG)是一种用来预防儿童结核病的预防接种疫苗。接种后可使儿童产生对结核病的特殊抵抗力,尤其对预防儿童粟粒性结核与结核性脑膜炎的功效尤为明显。我国规定新生儿出生后2~3 d内接种卡介苗,7岁复种,在农村12岁时再复种一次。但是卡介苗的作用也有其局限性,比如对成人的结核病预防作用就很弱,还不能完全防止结核病的发生。针对卡介苗存在的“先天缺陷”,随着相关学科的发展并借助各项生物技术,许多国家正在加紧研制新一代更为有效的抗结核菌疫苗。
卡介苗的质量与菌种有密切的关系。当前世界各地实验室所用卡介苗都直接或间接来自巴斯德研究所。菌种移种到各地之后,由于各种条件的变化,各自出现了与原株不同的特性,从而形成了当地的卡介苗亚株。在国际上曾被推广使用的有F1173P2株和D1331株。国际上曾多次进行卡介苗菌种的对比选择研究,专家们认为,在世界上还未找到两个具有同一特性的亚株,也没有经验证明哪个亚株对人不产生免疫力。在确定种子批菌种时,只要求在动物试验中能产生较好的保护力,在人群中能产生较高的结核菌素敏感性及较低的不良反应,菌株能适应当地实验室的条件及疫苗能被临床方面认可即行。
为了防止继续变异,WHO于1965年制定的冻干卡介苗制检规程中规定,生产卡介苗要采用种子批系(seed lot system)菌种,启开种子批菌种,不能超过12代,以保持其稳定性。我国现采用由上海生物制品研究所保存的丹麦823株(又称D2株)种子批菌种D2PB302S2甲10株作为生产株。
3.卡介苗的生产方法
卡介苗大多采用表面培养,少数采用深层培养。
(1)表面培养。
表面培养是卡介苗生产用的经典方法。
启开种子批菌种,接种于改良的苏通马铃薯培养基,培养温度为37~39℃,培养时间为2~3周,活化;在苏通马铃薯培养基上再传1代或直接挑取生长良好的菌膜,移种于改良苏通培养基或其他适宜培养基的表面,37℃静置培养1~2周,扩培;其菌膜可作为生产接种材料。挑取发育良好的菌膜移种于改良苏通培养基或其他培养基的表面,37℃静置培养8~10周,收获菌膜。菌膜收集后压平,移入盛有不锈钢珠的瓶内,加入适量稀释液,低温下研磨,研磨好的原液稀释成各种浓度,冻干制成成品。凡在培养期间或终止培养时,有菌膜下沉、发育异常或污染杂菌者,必须废弃。
采用改良的苏通培养基生产的卡介苗活力高。用培养6~8 d的幼龄菌,有利于生产冻干制品,采用对数生长期的幼龄培养菌代替平衡期培养菌来生产,可使活菌率由10%左右提高至30%~50%。
(2)深层培养。
世界上有英国、瑞士和荷兰的三个实验室用加吐温-80或Triton WR1339液体培养基对卡介菌进行深层培养,卡介菌在液体培养基中均匀地分散生长。
①液体培养基成分:每升无热原蒸馏水中含天冬酰胺0.5 g、柠檬酸镁1.5 g、磷酸二氢钾5.0 g、硫酸钾0.5 g、吐温-800.5 mL、葡萄糖10 g。
②种子培养:将保存于苏通培养基上的原代种子接入上述培养基中接种传代2次,于37℃培育7 d后移种。
③深层培养:将上述种子移至装有6 L培养基的8 L双臂瓶中,于37℃培养7~9 d,通气电磁搅拌。然后通过超滤,浓缩为10~15倍的菌苗,加入等量25%乳糖水溶液后混匀。以1 mL分装安瓿冻干,真空封口,贮于-70℃备用。
4.卡介苗生产基本要求
生产和检定用设备、原材料及辅料、水、器具、动物等应符合《中国药典》中凡例的有关要求。卡介苗生产车间必须与其他生物制品生产车间及实验室分开。卡介苗生产所需设备及器具均须单独设置并专用。卡介苗生产、包装及保存过程均须避光。
从事卡介苗生产的工作人员及经常进入卡介苗车间的人员,必须身体健康,经X射线检查无结核病,且每年经X射线检查1~2次,可疑者应暂离卡介苗的生产,其检查记录必须保存备查。生产用培养基不得含有能使人产生毒性或变态反应的物质。培养基所用的原料应符合《中国生物制品主要原材料试行标准》的规定。
5.种子批的制备
生产用菌种应符合生物制品生产检定用菌毒种管理规程的规定。
采用卡介菌D2 PB302菌株。严禁使用通过动物传代的菌种制造卡介苗。按照生物制品生产检定用菌毒种管理规程的规定建立种子批。工作种子批启开至菌体收集单批收获培养物的总传代数不得超过12代。种子批应冻干保存于8℃以下。
种子批菌种应具有良好的培养特性。在苏通培养基上生长良好,培养温度在37~39℃。抗酸染色应为阳性。在苏通马铃薯培养基上培养的卡介菌应是干皱成团、略呈浅黄色。在苏通培养基上卡介菌应浮于表面,为多皱、微带黄色的菌膜。在牛胆汁马铃薯培养基上为浅灰色黏膏状菌苔。在鸡蛋培养基上有突起的皱型和扩散型两类菌落,且带浅黄色。
种子批菌种还应通过毒力试验检测。用结核菌素纯蛋白衍生物皮肤试验(皮内注射0.2 mL,含10 IU)阴性、体重300~400 g的同性豚鼠4只,各腹腔注射1 mL菌液(5 mg/mL),每周称体重,观察5周,动物体重不应减轻;同时解剖检查,大网膜上可出现脓疱,肠系膜淋巴结及脾可能肿大,肝及其他脏器应无肉眼可见的病变。
种子批菌种也应进行有无毒分枝杆菌的试验。用结核菌素纯蛋白衍生物皮肤试验(皮内注射0.2 mL,含10 IU)阴性、体重300~400 g的同性豚鼠6只,于股内侧皮下各注射1 mL菌液(10 mg/mL),注射前称体重,注射后每周观察1次注射部位及局部淋巴结的变化,每2周称体重1次,豚鼠体重不应降低。6周时解剖3只豚鼠,满3个月时解剖另3只,检查各脏器应无肉眼可见的结核病变。若有可疑病灶,应做涂片和组织切片检查,并将部分病灶磨碎,加少量生理盐水混匀后,由皮下注射2只豚鼠,若证实系结核病变,该菌种即应废弃。若试验未满3个月而豚鼠死亡,则应解剖检查,若有可疑病灶,即按上述方法进行,若证实系结核病变,该菌种即应废弃。若证实属非特异性死亡,且豚鼠死亡1只以上时应复试。
种子批菌种必须经过免疫力测定试验。用种子批菌种制备疫苗,经皮下免疫体重300~400 g的豚鼠4只,每只注射0.2 mL(1/10人用剂量),对照组注射0.2 mL生理盐水。豚鼠免疫后4~5周,经皮下攻击103~104强毒人型结核分枝杆菌,攻击后5~6周解剖动物,免疫组与对照组动物的病变指数及脾脏毒菌分离数的对数值经统计学处理,应有显著差异。如无条件,可送中国食品药品检定研究院进行。
(二)确定生产技术、生产菌种和工艺路线
(1)确定生产技术:发酵法培养结核杆菌生产卡介苗技术。
(2)确定生产菌种:丹麦823株(又称D2株)种子批菌种D2PB302S2甲10株。
(3)确定生产工艺路线,如图1-10-3所示。
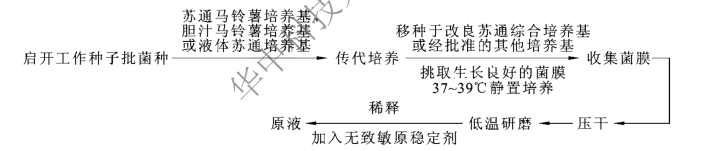
图1-10-3 卡介苗生产工艺路线
二、生产工艺过程
(一)卡介苗生产
1.生产用种子
启开工作种子批菌种,在苏通马铃薯培养基、胆汁马铃薯培养基或液体苏通培养基上每传1次为1代。工作种子批至单批收获培养物的总传代数不得超过12代。在马铃薯培养基培养的菌种置于冰箱中保存,不得超过2个月。
2.培养基
生产用培养基为苏通马铃薯培养基、胆汁马铃薯培养基或液体苏通培养基。
3.菌种接种与培养
启开工作种子批菌种培养1~2周,挑取生长良好的菌膜,移种于改良苏通综合培养基或经批准的其他培养基的表面,37~39℃静置扩大培养8~10周。培养过程中应每天逐瓶检查,如有污染、湿膜、混浊等情况应废弃。
4.收集和合并
培养结束后,应逐瓶检查,若有污染、湿膜、浑浊等情况应废弃。收集菌膜压干,移入盛有不锈钢珠的瓶内,钢珠与菌体的比例应根据研磨机转速控制在适宜的范围,并尽可能在低温下研磨。加入适量无致敏原稳定剂稀释,制成原液。
(二)质量检定
1.原液检定
(1)纯菌检查 活菌含量测定按生物制品无菌试验规程抽样做纯菌试验。也可用XTT方法快速检测卡介苗(BCG)制品中的活菌含量。其原理是细菌在代谢过程中,通过氧化还原反应将XTT还原为可溶性的高色产物甲臜(formazan),甲臜含量反映了细菌中的活菌数量。将该方法应用于卡介苗活菌含量的快速检测中,通过BCG参考品活菌含量和XTT有色产物吸光度值的标准曲线,根据未知样品的吸光度值,在此标准曲线上读出未知样品的活菌含量。
(2)菌体浓度的测定 菌体浓度与其吸光度大小有一定的关系。原液稀释10倍后,测其吸光度,通过吸光度大小来判断菌体含量的多少。除此以外,还应测定菌体的沉降率、活菌的数量和活力。
2.半成品检定和成品检定
检定项目包括鉴别试验、物理检查、水分、纯菌检查、效力测定、活菌数测定、有无毒分枝杆菌和热稳定性。除水分测定、活菌数测定和热稳定性试验外,按标示量加入灭菌注射用水,复溶后进行其余各项检定。
通过鉴别试验确定细菌形态与特性是否符合卡介菌特征。物理检查项目包括外观和装量差异。外观应为白色疏松体或粉末状,按标示量加入注射用水,应在3 min内完全溶解。装量差异应符合规定。水分含量应不高于3.0%。
效力测定选用经过结核菌素纯蛋白衍生物皮肤试验(皮内注射0.2 mL,含10 IU)阴性、体重300~400 g的同性豚鼠4只,每只皮下注射0.5 mg供试品,注射5周后皮内注射TB-PPD 10 IU(0.2 mL),并于24 h后观察结果,局部硬结反应直径应不小于5 mm。
每亚批疫苗都应做活菌数测定。抽取5支疫苗,稀释并混合后进行测定,培养4周后含活菌数应不低于1.0×106 CFU/mg。
有无毒分枝杆菌试验中,试验动物选用结核菌素纯蛋白衍生物皮肤试验(皮内注射0.2 mL,含10 IU)阴性、体重300~400 g的同性豚鼠6只,每只皮下注射相当于50次人用剂量的供试品,每2周称体重一次,观察6周,动物体重不应减轻;同时解剖检查每只动物,若肝、脾、肺等脏器无结核病变,即为合格。当动物死亡或有可疑病灶时,应做涂片和组织切片检查,并将部分病灶磨碎,加少量生理盐水混匀后,由皮下注射2只豚鼠,若证实是结核病变,该批产品就应作废。
取每亚批疫苗于37℃放置28 d测定活菌数,并与2~8℃保存的同批疫苗进行比较,计算活菌率;37℃的产品活菌数应不低于2~8℃本品的25%,且不低于2.5×105 CFU/mg。以此确定产品的热稳定性。所用稀释剂应为灭菌注射用水。
产品应于2~8℃避光保存和运输。自生产之日起,按批准的有效期执行。保质期一般为一年。
有关生物制药工艺(第2版)的文章

所以,目前还不能对发酵进行全面控制,使其按人的意志进行目标产物的生物合成。但是,掌握发酵工艺条件对发酵过程的影响以及微生物代谢过程的变化规律,可以帮助人们有效地控制微生物生长和代谢产物的发酵生产,不断提高发酵水平。此外,通过发酵动力学研究,建立能定量描述发酵的过程的数学模型,并借助现代过程控制手段,为发酵生产的优化控制提供技术和条件支持。......
2023-11-18

经过建库以来几代管理者的科学、精心管理,陡河水库工程一直处于良好的运行状态。坝顶防浪墙修复及照明线路敷设工程的竣工为大坝安全度汛和紧急情况下大坝照明提供了有力保障。配电室电气更换工程的完工为陡河水库安全用电、紧急用电提供了切实的保障。陡河水库大坝实现了计算机远程控制、自动控制、人工控制,大坝安全监测系统达到了自动化,提高了现代化管理水平。......
2023-06-18

正如上节所述,跨流域调水工程设计通常有许多不同的方案,而各种设计方案的评估是个非常复杂的问题。显然,从工程投资、社会经济效益和生态环境保护费用三方面考虑,并非所有方案都同样地引人注意,问题是要寻求最优方案。使用线性规划或其他类似的方法筛选了一系列方案后,下一阶段就是以最优方案为基础进行系统设计。所以,提出跨流域调水“最优运行规则”也许是不合适的,而应该采用“满意”方案。......
2023-06-30

建有功能安全保护系统,采用全生命周期方法有效避免系统失效。在石油开采、石化化工、钢铁、有色金属、稀土材料、建材、纺织、食品、医药、造纸等流程制造领域,企业可以开展智能工厂的集成创新与应用,可以提升企业在资源配置、工艺优化、过程控制、产业链管理、质量控制与溯源、能源需求侧管理、节能减排及安全生产等方面的智能化水平。......
2023-06-28

贾爱娟等指出环境相关评价与清洁生产评价不同,前者的目标在于显示/表示环境品质的状况,后者则是界定一个生产工艺或产品的清洁生产状况。崔元贵则从清洁生产技术投入的角度构建清洁生产指标函数。清洁生产测度指标的作用不仅体现在检测产品或服务生产过程的清洁水平上,更关键的是诊断生产过程中的“不清洁”因素。沈鹏等提出的清洁生产评价指标可以帮助企业进行污染全过程控制,使各个生产环节的污染测度具体化和定量化。......
2023-06-20

由于在前文11.3.2节确定9月份分旬控制水位时并未考虑泥沙淤积的影响,但实际上,随着三峡水库运用时间的增加,水库淤积不断增长,泥沙淤积将造成防洪库容损失,对原定分旬控制水位产生影响。具体做法是:根据一维数学模型计算结果,淤积在三峡水库145~175m 高程之间的泥沙为36亿m3,保留防洪库容为185亿m3,占原来防洪库容的83.7%。表11-13淤积平衡后分旬控制蓄水平均年增加的发电量......
2023-06-23

发酵工程按人类对微生物技术的利用程度可分为如下阶段。(一)天然发酵时期人类利用微生物的代谢产物作为食品,已有几千年的历史。青霉素发酵技术的迅速发展推动了抗生素工业乃至整个发酵工业的发展。传统的发酵技术,与现代生物工程中的基因工程、细胞工程、蛋白质工程和酶工程等相结合,使发酵工业进入到微生物工程的阶段。......
2023-11-18

通常不产芽孢的,也不产多黏菌素。图2-2-1多黏菌素E发酵生产工艺流程表2-2-2多黏菌素E发酵生产工艺条件图2-2-1多黏菌素E发酵生产工艺流程表2-2-2多黏菌素E发酵生产工艺条件确定详细的发酵工艺,包括通气量、二阶段发酵温度、最适生长温度和pH、最适生产温度和pH、发酵时间、补料及消泡剂等。......
2023-06-24
相关推荐