本节以最为常用的电磁感应水冷铜坩埚凝壳熔炼为例,介绍钛合金熔炼时的基本特征。由图可知,开始保温之后,随着保温时间的延长,凝壳质量分数fskull急剧减小,这是因为输入的能量大于熔体通过冷坩埚和热辐射损失的能量,使得之......
2025-09-29
2.1.4.1 冲天炉内冶金环境
(1)冲天炉内的气相
1)气相的成分。表2-9列出了冲天炉加料口处炉气成分的范围。其中SO2的含量(体积分数)和H2O的含量根据焦炭每含1%的S,产生0.1%SO2,每含1%的水,产生0.2%水蒸气估计。
表2-9 加料口处炉气成分(ηv=40%~90%)

CO2和CO的计算见式(2-42)、(2-43)。
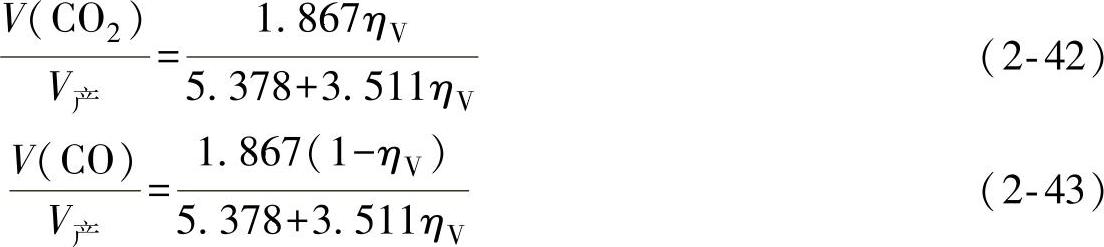
如图2-23所示为CO和CO2在CO2-CO-C-Fe平衡图上浓度随炉温变化的情况。两条实线是划分FeO稳定区的边界线。两条线中间的区域是FeO的稳定区。在该区域以上,为Fe的稳定区,该区域的下部为Fe3O4的稳定区;
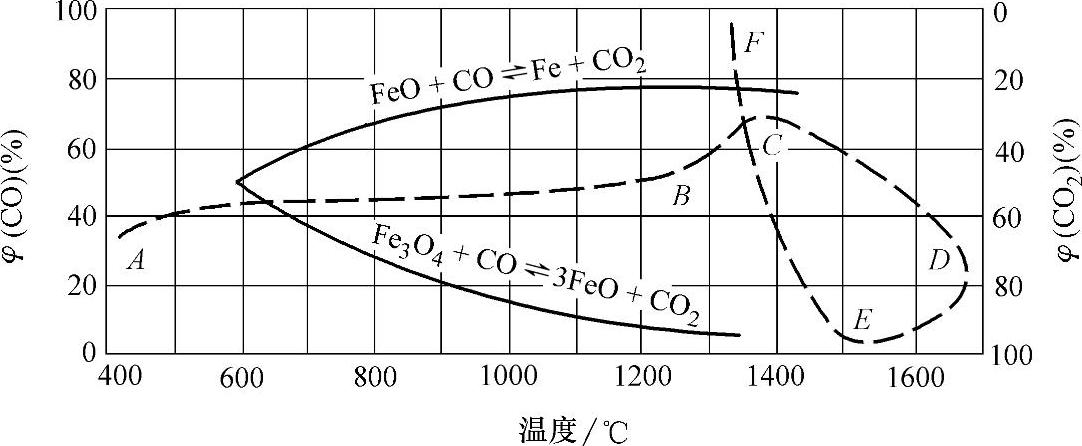
图2-23 炉气在CO2-CO-C-Fe平衡图的位置
2)炉气的化学性质。O2和CO2对碳和合金元素都是氧化性气氛,CO对金属的氧化性较弱,对某些金属具有还原性。
(2)冲天炉内的渣相
1)渣的成分见表2-10。
表2-10 冲天炉炉渣成分
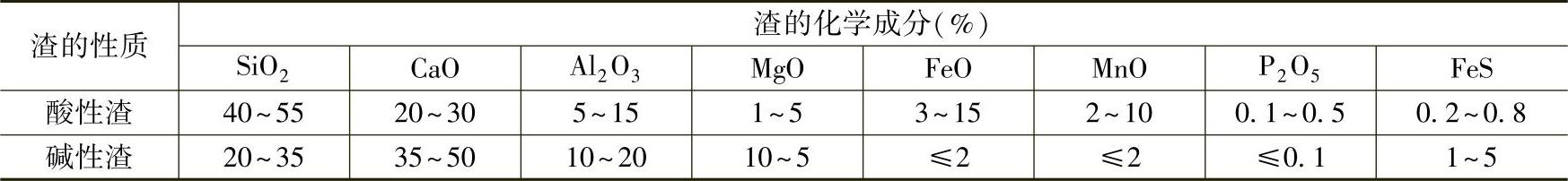
2)炉渣的性质
①渣的黏度。渣的黏度随着温度升高而下降,降至2.0~2.5Pa·s时,渣即可自由流动。图2-24所示为不同成分炉渣的熔化性温度(渣达到自由流动的温度),可供调整渣成分及温度的参考。
②渣的化学特性
a.炉渣的碱度。表示炉渣酸碱性的参数是炉渣的碱度,记为

w(CaO)、w(MgO)、w(SiO2)、w(Al2O3)分别表示该氧化物在渣中的质量分数。Al2O3为两性氧化物,在酸性渣中呈现碱性,在碱性渣中呈现酸性,通常在酸性渣中不计入Al2O3的量,而在碱性渣计算中,将Al2O3作为酸化氧化物计入。表2-11列出了不同性质炉渣的碱度。
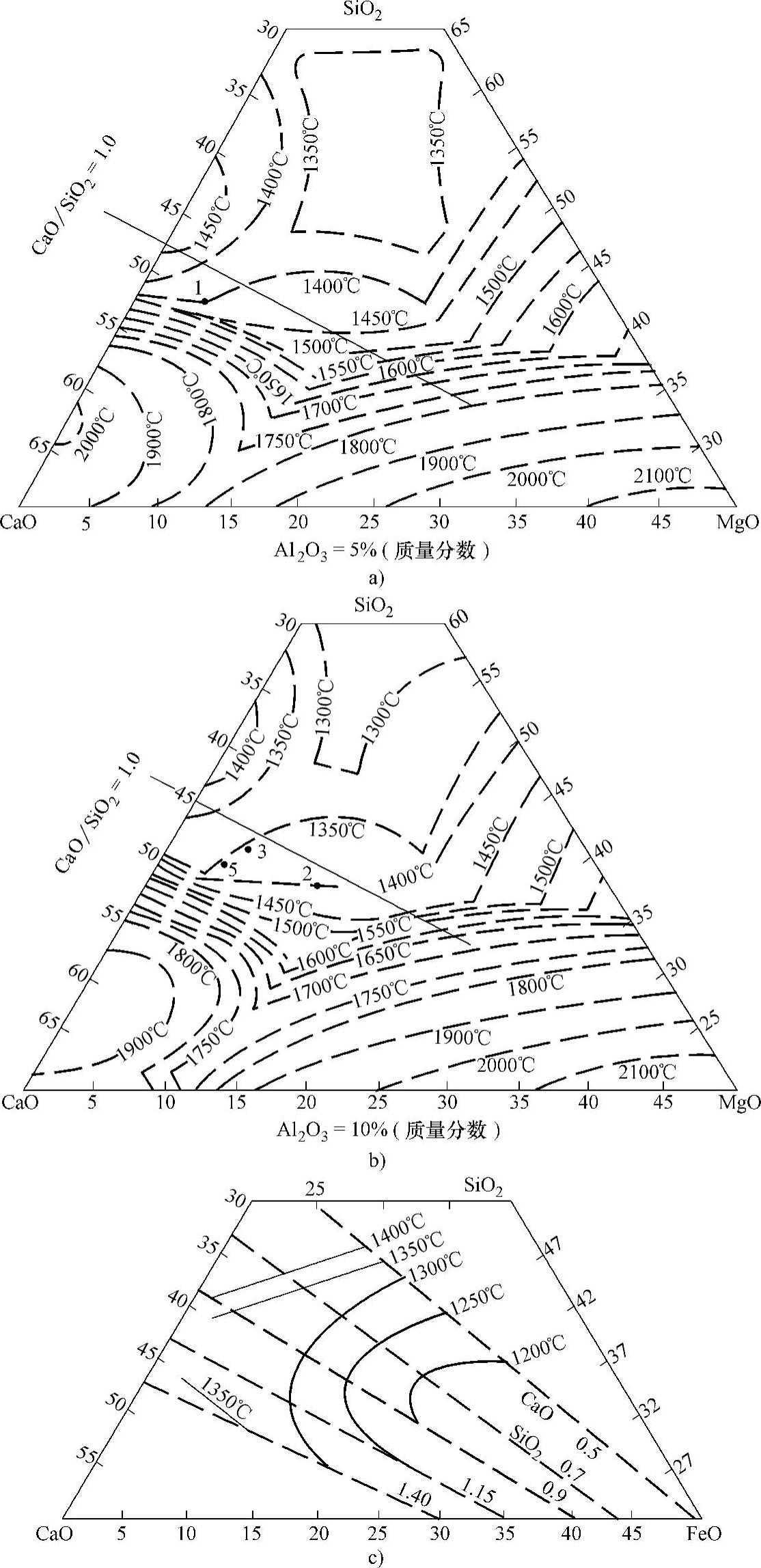
图2-24 渣的成分与熔化性温度
a)CaO-SiO2-MgO-Al2O3四元系炉渣 b)CaO-SiO2-MgO-Al2O3四元系炉渣 c)CaO-SiO2-FeO渣系(Al2O3=9%(质量分数);MgO=7.5%(质量分数);MnO=1.5%(质量分数))
表2-11 不同碱度炉渣的性质

b.炉渣的氧化性。铁液中金属元素被渣中的氧所氧化,渣中氧向铁液中转移的现象为渣的氧化性,可用渣—铁平衡时铁液的含氧量[O]O与铁液实际含氧量[O]S之差表示
Δ[O]=[O]O-[O]S
当Δ[O]=0时,渣—铁之间没有氧的转移;当Δ[O]>0时,渣为氧化性;当Δ[O]<0时,铁液中的FeO被还原,渣为还原性。渣—铁之间氧的转移主要通过FeO的转移来实现。
(3)冲天炉内的焦炭。焦炭以固态处于冲天炉的冶金环境中,冶金反应在焦炭表面进行,因此焦炭表面的性质直接关系到焦炭的冶金性能。影响焦炭表面性质的因素包括块度、反应性、固定碳含量、杂质种类和含量等。
2.1.4.2 冲天炉内铁液成分的变化
1.碳的变化
(1)铁液的氧化脱碳
1)被炉气中的CO2氧化:[C]+CO2→2CO,此反应为吸热反应,随温度升高而加剧。在冲天炉条件下,只要炉气中有CO2存在,反应都会进行。
2)被炉气中的O2氧化。能产生此反应的是氧化带,这里有氧气,铁是液态,C在铁液中的扩散迅速,而氧气大多被焦炭燃烧耗掉,形成很高的温度,到达铁液表面的O2的浓度不高,反应为:2[C]+O2→2CO,生成CO进入炉气中。
3)被渣中氧化铁氧化。[C]+FeO→[Fe]+CO,反应在铁液与渣液界面进行,产生的还原铁溶入铁液中,CO进入炉气。
铁料在熔化带一开始熔化即会被渣中FeO氧化脱碳,表面锈蚀的铁料会增加渣中的FeO含量,导至铁液脱碳加剧。
4)被铁液中溶解氧氧化。[O]+[C]→CO,生成的CO进入炉气中。反应在铁液表面和铁液与焦炭、炉壁接触的利于CO析出的固相界面进行。
铁液中碳的氧化是放热反应,温度偏低时反应更强烈。所以熔化带是铁液更容易脱碳的区域,当熔化带呈氧化性气氛时,刚熔化的铁液将被剧烈氧化脱碳。
(2)铁液增碳 碳溶入铁液的反应可用下式表示
3Fe(液)+C(固)→Fe3C(液)-Q
反应在铁液与焦炭或增碳剂的界面进行。溶入铁液表层的碳向内扩散,进入铁液内部,碳向铁液内部渗入的速度可用式(2-45)表示

式中 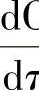 ——渗碳速度,表示单位时间铁液中碳浓度的增量;
——渗碳速度,表示单位时间铁液中碳浓度的增量;
D——随温度升高而增大的碳在铁液中的扩散系数;
F——铁液与焦炭接触面积;
V——铁液体积;
δ——扩散层厚度;
w(C)——铁液中碳的实际质量分数;
w0(C)——铁液中碳的饱和质量分数。
铁液中饱和溶碳量趋于共晶碳量4.3%,但由于铁液中其他元素对碳在铁液中溶解度的影响,实际含碳量往往低于4.3%。如图2-25所示为常见元素对铁液中碳溶解度的影响。
表2-12为在铁碳溶液中加入1%(质量分数)元素X引起碳在铁液中溶解度的改变值ΔC。
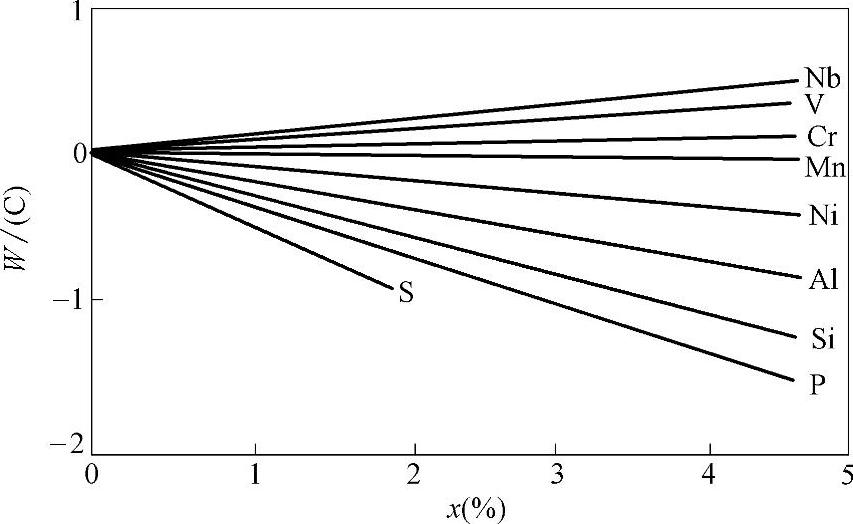
图2-25 合金元素对碳在铁液中溶解度的影响
表2-12 铁碳溶液中加入1%(质量分数)元素X引起碳在铁液中溶解度的改变值ΔC

从表中可见,在铸铁的五大元素中,Si、P、S对碳在铁液中的溶解度影响最大,但S的含量通常很低,其影响可忽略不计。铸铁中碳的饱和溶解度可近似表为式2-46
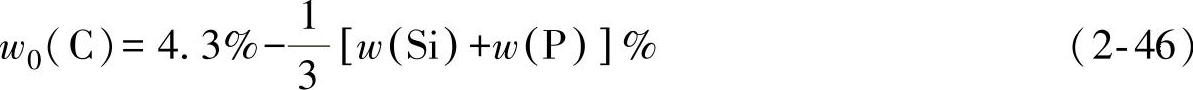
(3)影响铁液中碳含量的因素
1)铁料的成分。铁料中的碳含量越接近共晶碳量,铁液中增碳量越少,反之,可以溶入的碳量越多。
2)焦炭。固定碳含量越高、铁液与焦炭接触面积越大、焦炭表面越洁净、焦炭表面气相的氧化性越弱、铁液与焦炭接触时间越长、铁液流股越薄则越有利于铁液增碳,反之则不利。因此,块度小、灰分少、含S低、反应性高的焦炭,有利于铁液增碳。
3)送风条件。图2-26反映了送风强度对铁液增碳的影响,提高送风强度,铁液的增碳量下降。图2-27所示为冲天炉熔化强度对铁液含碳量的影响。
提高风温和风中O2的浓度、适当提高风速,对铁液增碳是有利的。风中可燃性杂质能强化CO的燃烧,增强炉气的氧化性,对铁液增碳不利,但由于强化底焦燃烧使炉温提高,在一定程度上减弱了这种不利影响。
风中水分的影响类似于可燃性杂质。过量的水蒸气不但加剧氧化性,还会降低炉温,从而促使铁液氧化脱碳。
4)炉渣。适当提高渣的碱度,有助于清除焦炭表面酸性渣膜,有利于铁液增碳。但另一方面,铁液在炉内被氧化生成的FeO对碳有氧化作用。当炉渣碱度提高,比较反应
CaO+SiO2→CaSiO3 ΔG°1=-83320-3.43T
和SiO2+2FeO→Fe2SiO4 ΔG°2=-39360+14.2T可见:ΔG°1<ΔG°2,生成CaSiO3的反应更易于进行,生成的CaSiO3更稳定。所以随着CaO的增加,使得SiO2难于生成FeSiO4而使FeO增多,铁液中碳被氧化的趋势增强。在酸性炉中,由于渣中的SiO2量较大,增加CaO后带来的FeO量增加的影响并不明显。
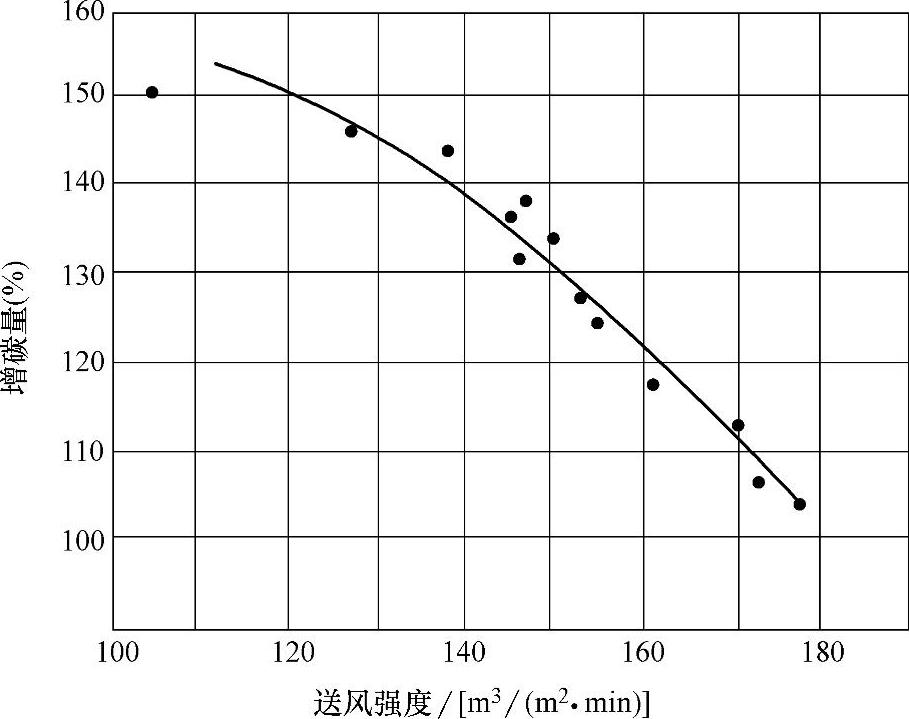
图2-26 送风强度对铁液增碳量的影响
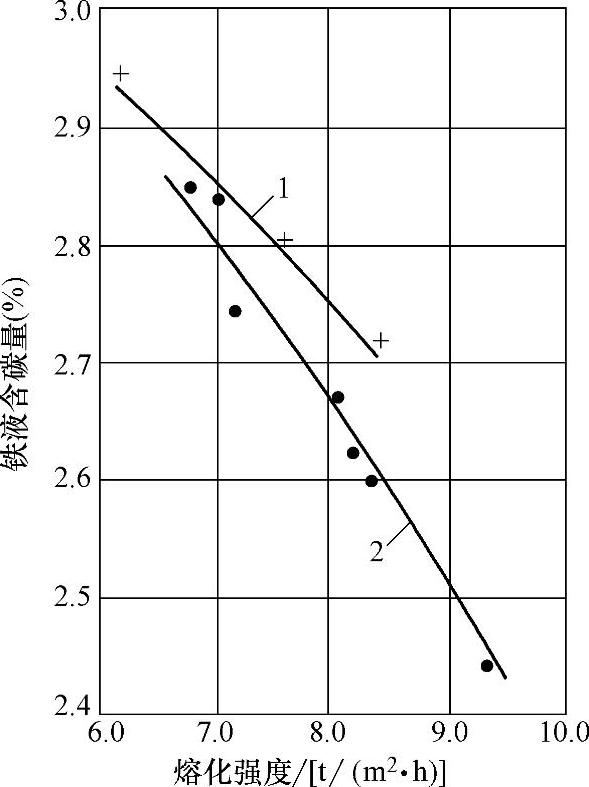
图2-27 熔化强度对铁液含碳量的影响
1—炉料含碳量1.35% 2—炉料含碳量1.15%
5)炉子结构。多排风口不利于铁液增碳,而单排风口有利于铁液增碳。闭渣口操作时,越深的炉缸,对铁液的增碳作用越强。对于存留铁液的炉缸结构,会造成铁液的大量增碳。
6)操作工艺。开渣口操作不利增碳,在炉缸内投放增碳剂,及时排放前炉内熔渣,减少渣内FeO,减少因渣中硫分向铁液渗入而降低铁液中碳的溶解度,对出炉铁液采用覆盖剂防止氧化烧损碳分等操作都有利于增碳。
2.金属元素的变化
(1)Si的变化
1)Si的氧化
①被炉气中自由氧氧化。[Si]+O2→(SiO2),随着温度的升高,反应减弱;随着O2分压和Si的浓度上升、SiO2浓度的下降反应加剧。
②被炉气中CO2氧化。[Si]+2CO2→(SiO2)+2CO,随着温度和CO分压力的降低、CO2分压力的上升,反应趋势增强。在底焦中的不同区带,Si被CO2氧化的反应都能自发进行。
③被FeO氧化。[Si]+2FeO→2[Fe]+(SiO2),炉温低、渣的碱性大,反应增强。
④被铁液中溶解的氧氧化。2[O]+[Si]→(SiO2),反应随铁液温度的提高而减弱,随铁液中氧、硅浓度提高和渣中二氧化硅浓度的降低而增强。
2)SiO2的还原。图2-28所示为冲天炉内SiO2被C还原的自由能变化。
①被焦炭中C还原。(SiO2)+2C→[Si]+2CO,反应的程度除受温度影响外,还随着渣中二氧化硅浓度的提高和铁液中硅浓度的降低而增强。
②被铁液中的C还原。(SiO2)+2[C]→[Si]+2CO,反应需要高温条件和还原性气氛。
在一般冲天炉中,Si的氧化趋势大于SiO2的还原趋势,所以铁液中的Si通常是烧损的。在单排风口外热风冲天炉中,Si的烧损通常不高于5%(质量分数),甚至可以增硅。
(2)Mn变化
1)Mn的氧化
①被自由氧氧化。2[Mn]+O2→2(MnO),为放热反应,随温度的升高反应趋势减弱。在冲天炉内有自由氧存在的区域,反应都能自发进行。进行的程度随铁液中锰的浓度和炉气中氧的分压的提高、渣中氧化锰浓度的降低而增强。
②被铁液中溶解氧氧化。[O]+[Mn]→(MnO),随着铁液中Mn含量和溶解氧浓度的提高,反应趋势增强。
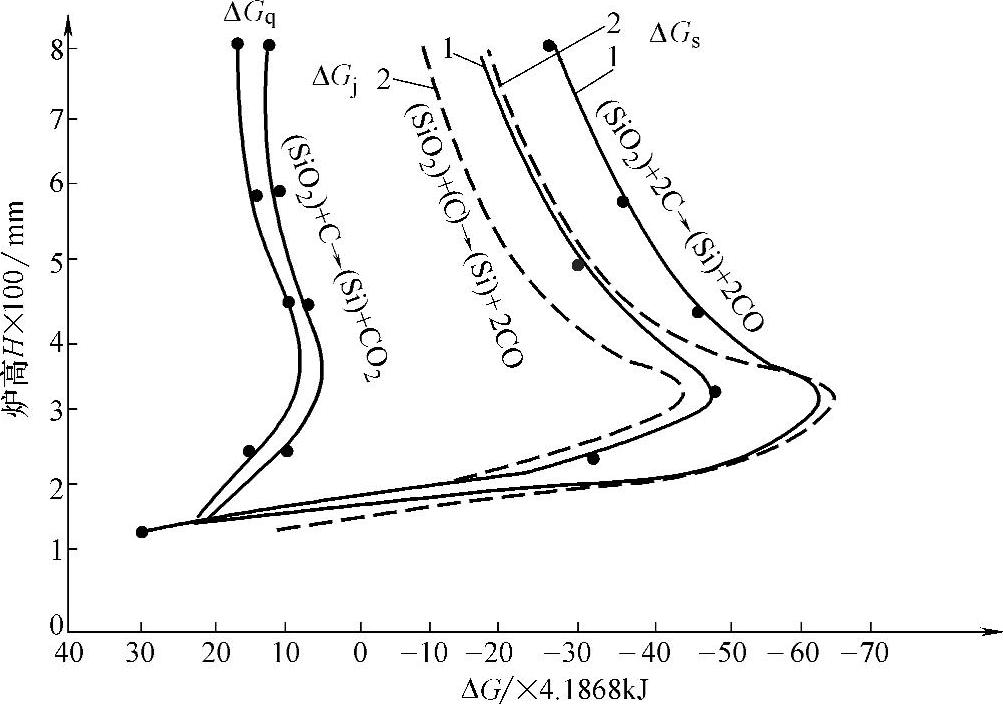
图2-28 冲天炉内SiO2被C还原的自由能变化
1—低风速 2—高风速
③被炉气中CO2氧化。[Mn]+CO2→(MnO)+CO,反应可以自发进行。
④被渣中FeO氧化。[Mn]+(FeO)→[Fe]+(MnO),反应可自发进行。随着温度的升高反应趋势减弱,渣中FeO含量和铁液中Mn量提高,都会使反应趋势增强。在酸性炉中,由于渣中FeO较多,Mn的烧损达20%~25%。
2)MnO的还原。MnO在冲天炉内的还原介质,只能是C,而不可能是CO,还原MnO的C来源于焦炭和铁液。
①被焦炭中的碳还原。(MnO)+C→[Mn]+CO,平衡温度T=1484K(1211℃)。温度高于1211℃反应有自发进行的可能。
②被铁液中碳还原。(MnO)+[C]→[Mn]+CO,在冲天炉底焦中,渣中MnO有被铁液中碳还原的趋势,随着铁液中碳量和渣中MnO量的升高,尤其温度的升高,反应的趋势增强。
从图2-29中可看出:渣中MnO被焦炭或铁液中C还原的反应,ΔG<0,可以自发进行,而铁液的C还原MnO的趋势稍弱于焦炭。
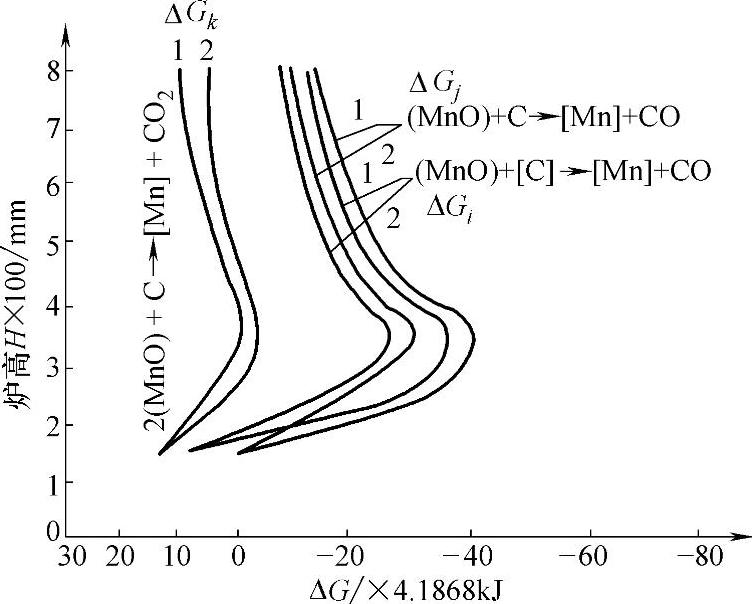
图2-29 MnO被C还原反应自由能变化
1—低风速 2—高风速
与氧亲和力越大的金属元素,氧化烧损的趋势越大,其氧化物还原的趋势越小。按金属元素氧化反应标准自由能变化的大小,可将冲天炉铁液中常见金属元素按与氧亲和力从小到大排列如下:Cu、Ni、W、Mo、Fe、Cr、Mn、V、Si、Ti、B、Al、Ce、Ca,该规律从图2-30中也可看出。
3)影响铁液中金属元素变化的因素
①温度。与炉气气氛相比,温度对金属元素的氧化、还原反应影响更大。提高温度为金属氧化物的还原反应加强了热力学条件,使金属氧化物还原的趋势增强,在一定的条件下,金属氧化物还原增加的金属元素量可能超过其氧化烧损量,出现铁液中合金元素增加的现象。
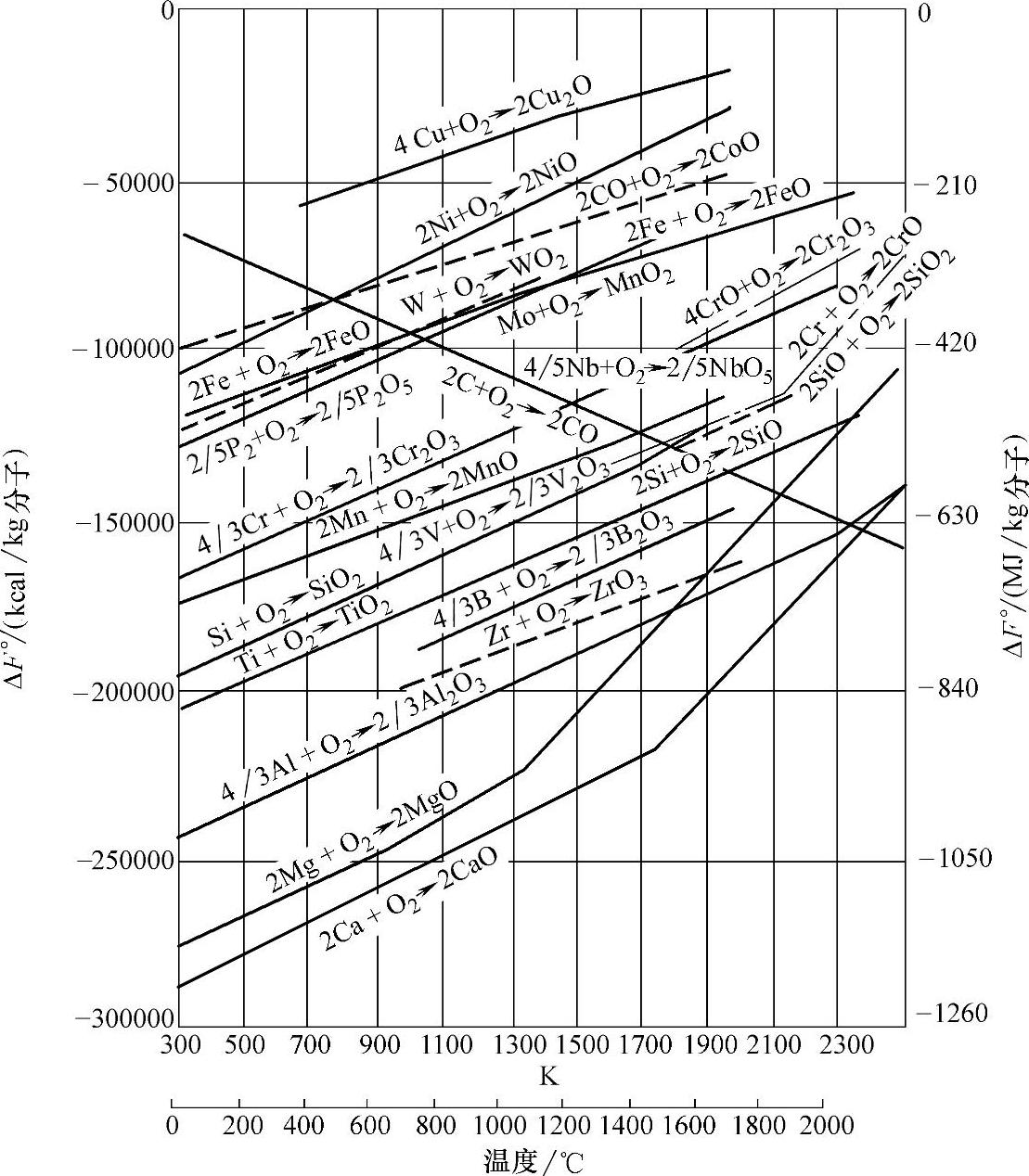
图2-30 氧化物标准生成自由能随温度的变化
②炉气中氧及二氧化碳。炉内O2和CO2浓度越高,分布的范围越广,对金属元素的氧化作用越强。图2-31反映炉气中CO2浓度对Si、Mn烧损率的影响。
③金属炉料。金属炉料中合金元素含量越高,与氧化剂接触的几率越高,则被氧化烧损的越多。有资料表明,当铁液中Mn的质量分数为1%~1.5%时,烧损15%~20%;含Mn的质量分数为1.5%~2%时,烧损增至20%~25%。表2-13为Si在炉料中含量与其烧损的比例。(https://www.chuimin.cn)
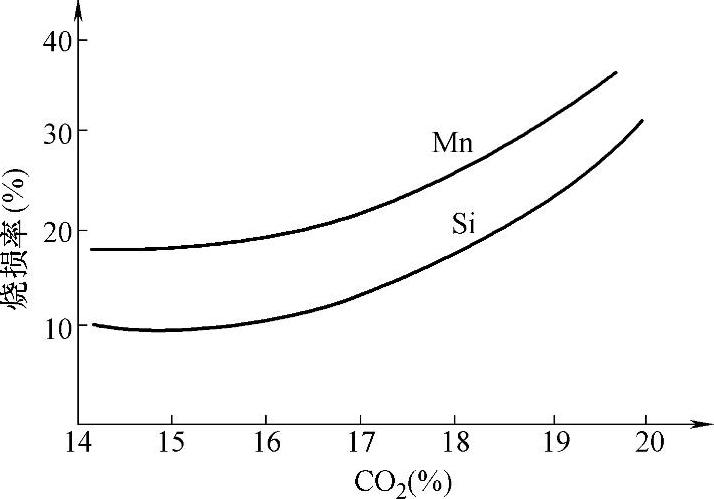
图2-31 炉气中CO2浓度对Si、Mn烧损的影响
表2-13 Si的烧损量与炉料中Si含量的关系

锈蚀的炉料由于带入了金属的氧化物,会烧损与氧亲和力更大的元素,所以锈蚀越严重的炉料,某些元素的烧损越严重。
④炉渣。炉渣中SiO2质量分数为40%以上,SiO2能与碱性氧化物MnO、CaO等生成低熔点盐,使自由态碱性氧化物浓度下降,有利于碱性氧化物的生成,从而加重金属元素的烧损。例如Mn与氧的亲和力不如Si,但在酸性炉中,由于MnO减少,有利于Mn的氧化反应,Mn的烧损反而比Si高。在碱性炉中,通常渣为碱性。CaO等碱性氧化物含量高,而SiO2的含量较低,Si的烧损则比Mn高。
3.铁液含硫量的变化
(1)增硫
1)金属炉料的增硫。硫的来源主要是焦炭,焦炭中的硫以有机化合物形式存在的约占65%~70%;以FeS、CaS等无机化合物存在的约占25%~30%;以硫酸盐形式存在的不到10%。在熔炼过程中,焦炭中的硫分将发生如下变化:FeS溶入铁液,CaS进入炉渣,S的有机化合物燃烧生成SO2,硫酸盐分解产生SO2都进入炉气中,遇金属炉料可发生反应
SO2+3Fe→FeS+2FeO+363010 J/mol(SO2);
10FeO+SO2→FeS+3Fe3O4
两个反应在冲天炉中都能自发进行;从FeO的变化看,前一个反应生成的FeO为后一个反应提供了条件;尤其当炉料表面FeO较多时,将加剧后一个反应的进行,使铁料渗硫量增加。渗硫反应在预热带下部进行得最激烈,铁料的渗硫层厚度通常达1~3mm。
2)铁液的增硫。铁液在流经焦炭表面时,焦炭中的FeS向铁液中溶解,这是铁液增硫的主要途径;炉气中的SO2在铁液表面也会与Fe及FeO发生上述两个反应,生成FeS溶入铁液。
(2)影响铁液增硫的因素
1)焦炭的影响。凡是能增加铁焦接触和铁硫接触的因素都会使铁中的渗硫量增加,如较高的焦炭含硫量,较小的焦炭块度、较高的反应性等。底焦高度和焦耗量的提高增加了铁碳的接触,也会促进铁液增硫。
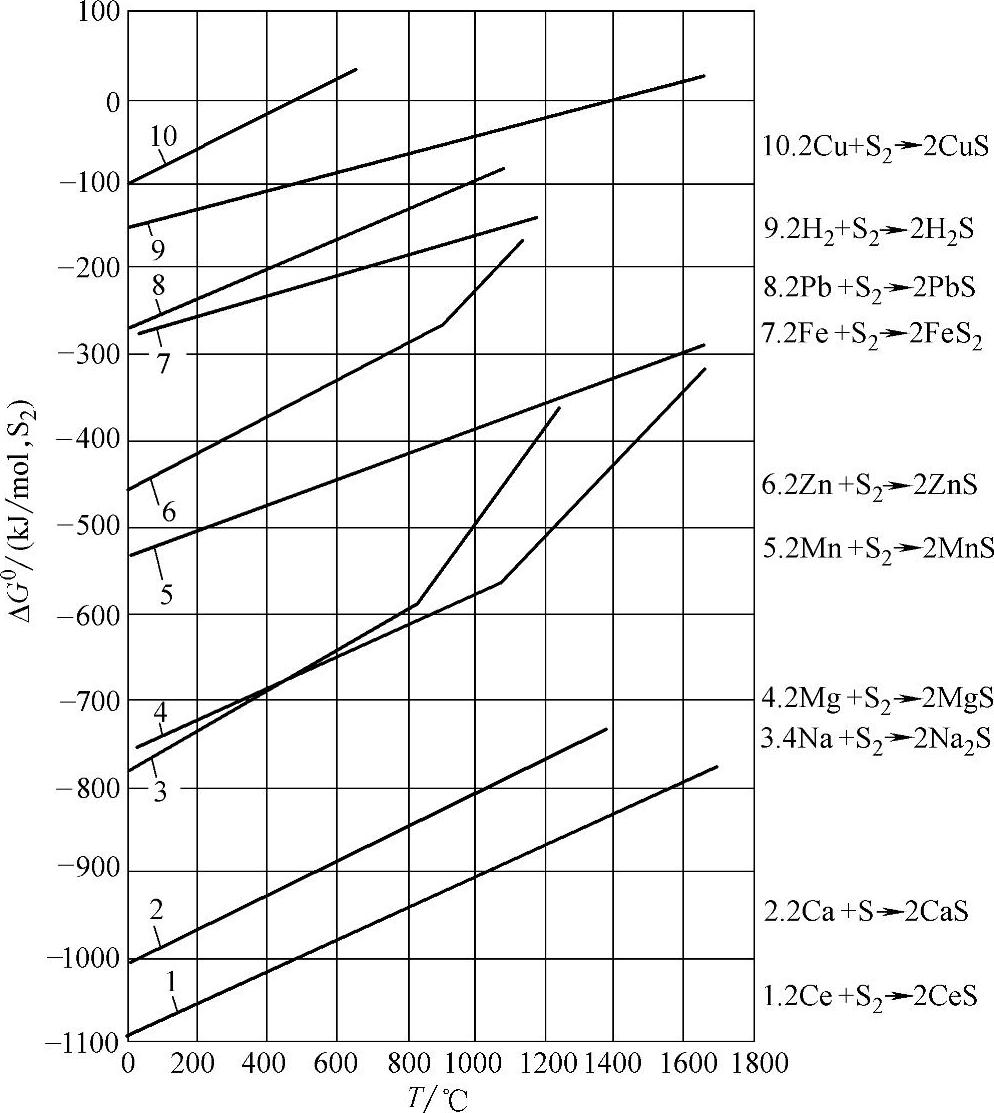
图2-32 硫化物标准生成自由能与温度的关系
2)温度的影响。图2-32表明,铁液渗硫反应的趋势随温度的升高而减弱。
3)炉料的影响。如图2-33所示,炉料中废钢的比例越高,增硫量越大。
炉料中的FeO使铁液增硫,所以锈蚀的炉料、细薄的炉料,尤其是钢切屑和轻薄钢料都会加重铁液的增硫,图2-34反映了
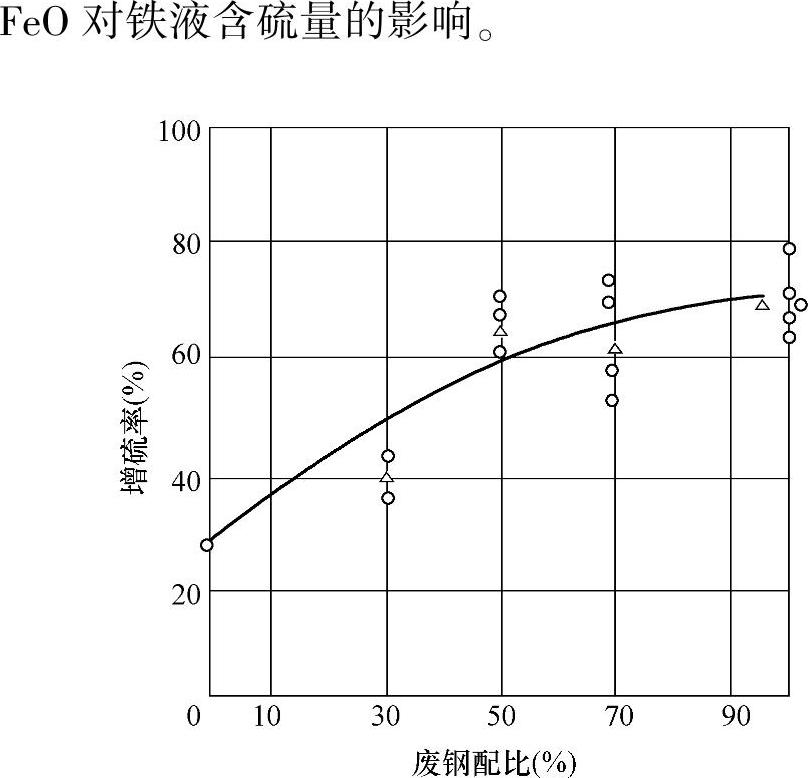
图2-33 炉料中废钢配比对铁液增硫率的影响
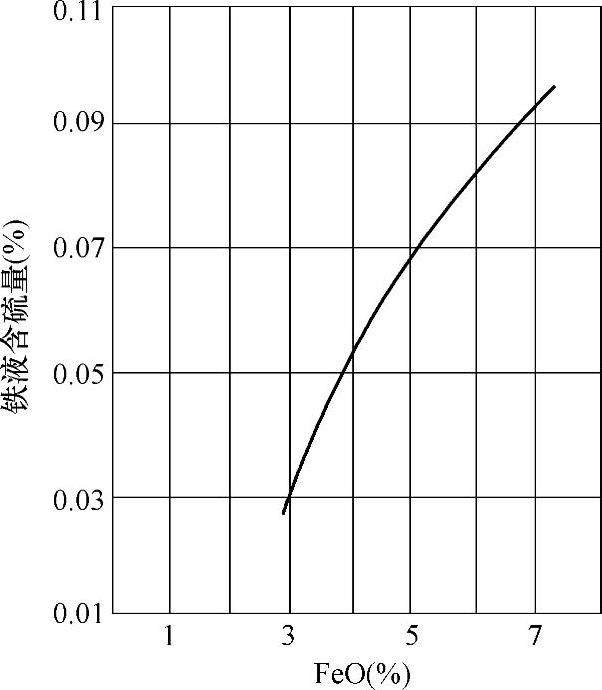
图2-34 渣中FeO对铁液含硫量的影响
4)渣的影响。硫化物存在于铁液中和渣中,在一定温度下,当铁液和渣液的成分一定时,硫在渣和铁液中的质量分数比例也是一定的。该比例称为硫的分配系数,也称作脱硫指数,记为

可见LS越大,渣中S的浓度越高,而铁液中的S的浓度越低。渣中的硫主要以CaS为主,铁液中的S以FeS为主。在渣与铁液的界面上,可发生反应
(CaO)+〔FeS〕→(CaS)+(FeO)-Q
反应的平衡常数可表为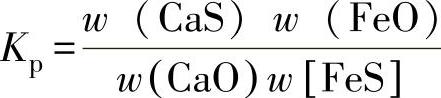 ;
;
CaS中的S含量为44.44%;S在FeS中的含量为36.47%,
由此 
该式表明S的分配系数与渣中CaO和FeO浓度有密切关系,LS随着w(CaO)的升高和w(FeO)降低而增大。图2-35表示炉渣碱度与LS的关系;随着炉渣碱度的增大,LS呈快速上升的趋势。如图2-36所示为渣中FeO对LS的影响,显示了LS随渣中FeO的增加而下降的趋势。
(3)铁液脱硫
1)铁液炉内脱硫。炉内脱硫的一般原则是高温、高碱度渣、低氧化铁含量。
①炉渣脱硫。炉内脱硫的主要反应[FeS]+(CaO)→(CaS)+(FeO),除了CaO,渣中还有能脱硫的其他碱性氧化物,用离子反应式可更全面地表达渣的脱硫过程
[S]+(O2-)→(S2+)+[O]
参与反应的(O2-)均来源于渣中的碱性氧化物。反应的平衡常数为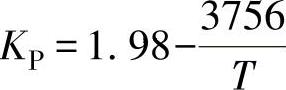
图2-37反映了渣的碱度越高脱硫能力越强。
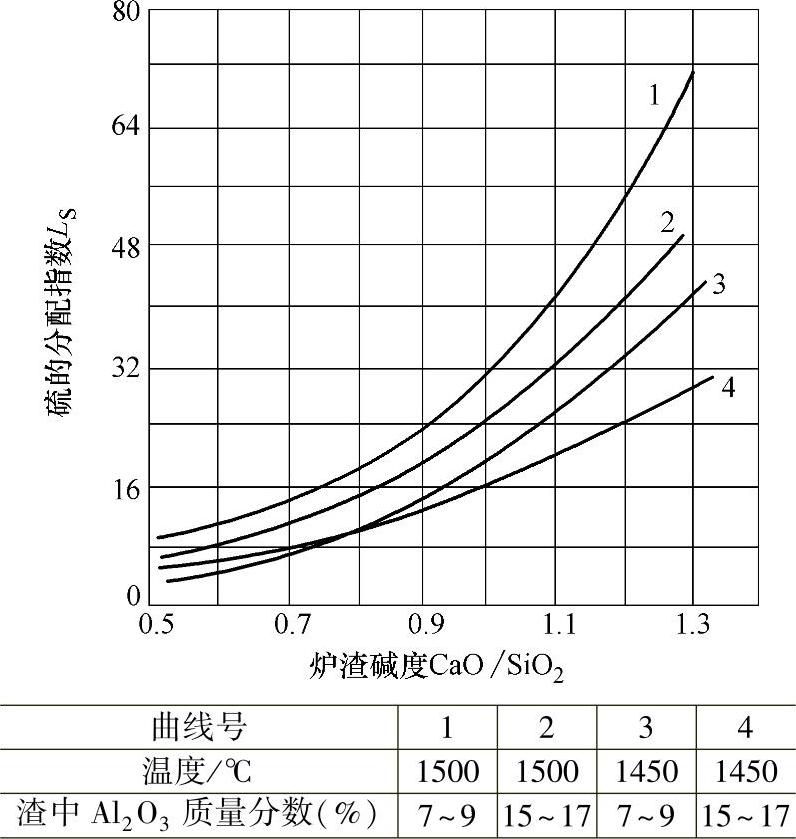
图2-35 LS与渣的碱度的关系
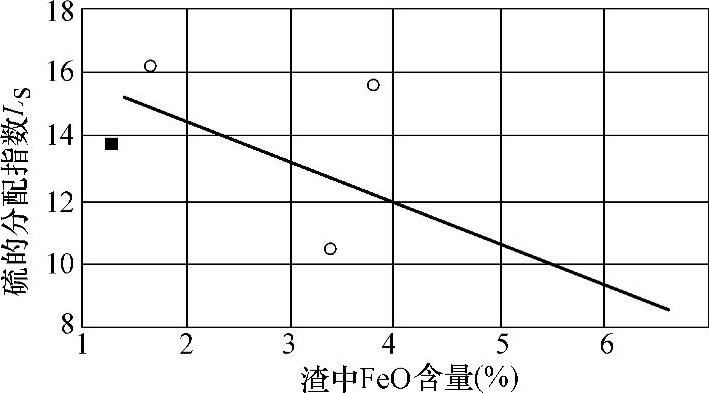
图2-36 硫的LS与渣中FeO含量的关系CaO/SiO2=1.3~1.4
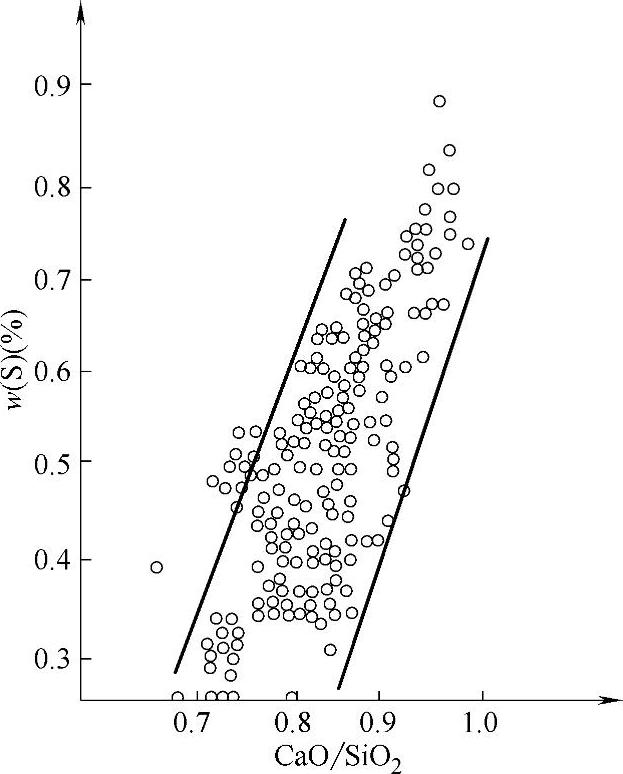
图2-37 炉渣中硫的浓度与炉渣碱度的关系
温度升高使铁液和渣的黏度下降,流动性增强,可提高炉内脱硫效果。
硫的分配系数LS反映了渣容纳硫的能力,可用容硫量表示。为计算渣的脱硫能力,令渣与硫的反应为
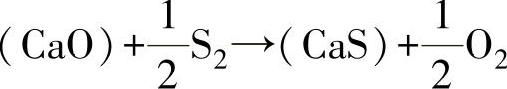
设渣中硫的质量分数为w(S),O2和S2的分压力为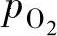 和
和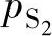 ,有如下关系
,有如下关系
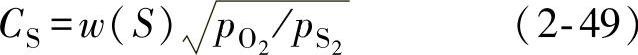
CS称为炉渣的容硫量。CS随渣中CaO活度的增大而增大,随CaS活度增大而减小。试验测得的高炉炉渣碱度R与lgCS的关系如图2-38所示,可供分析冲天炉脱硫问题参考。线性方程为
lgCS=-5.57+1.39R (2-50)
式中 R——渣的碱度。
酸性冲天炉造弱碱性渣可脱硫20%~30%以上;碱性冲天炉造碱性渣可脱硫50%~80%。
②金属元素脱硫 铁液中,Mn、Mg、稀土元素和钙等都有很好的脱硫效果。能脱硫的金属元素与氧的亲和力也大,在冲天炉内将被严重氧化烧损,因此金属元素并不作为脱硫剂加入冲天炉内,通常在炉外使用。金属元素的脱硫反应具有共性,现以Mn、Mg的脱硫反应为例进行说明。
Mn与铁液中的硫发生反应
[Mn]+[S]→(MnS)
MnS的熔点是1803K(1530℃)。反应的平衡常数分别是
T<1803K: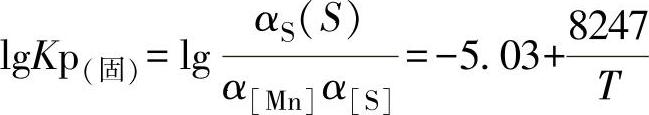
T>1803K: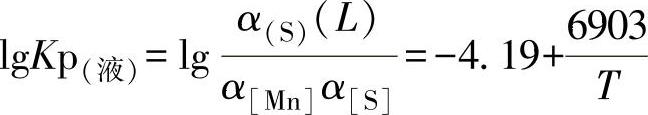
T=1803K:Kp(固)=1.633;Kp(液)=0.395。
Mg与S的亲和力很大,加入铁液中的固体Mg即与S发生反应,生成不溶于铁液的MgS
Mg(固)+[S]→MgS(固)
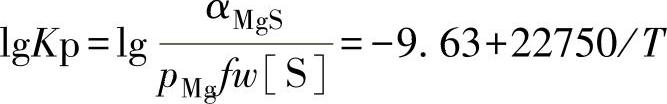
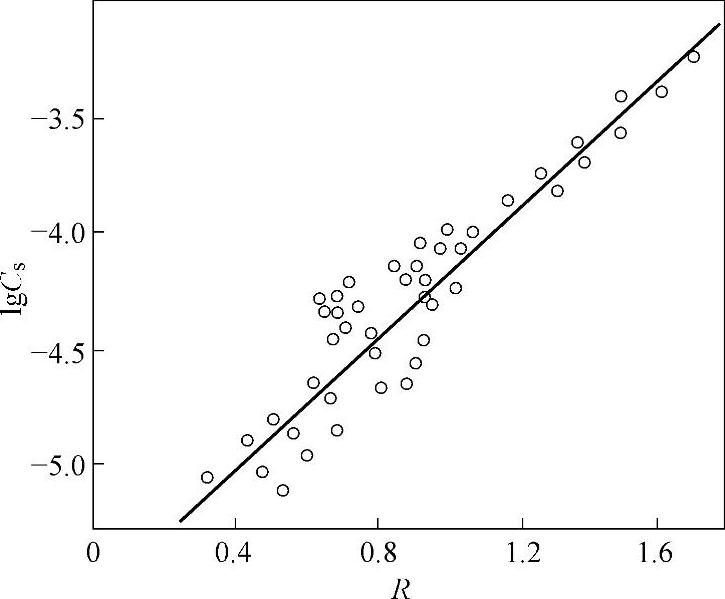
图2-38 炉渣容硫量与渣碱度的关系
溶解在铁液中的Mg与硫的反应是
[Mg]+[S]→MgS(固)
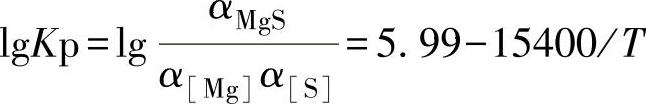
Mg在铁液中的饱和溶解度w0[Mg]:lgw0[Mg]=lgpMg-5.1+7000/T:
Mg在铁液中的蒸气压pMg: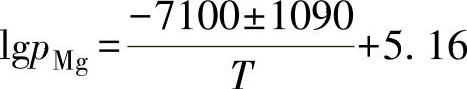
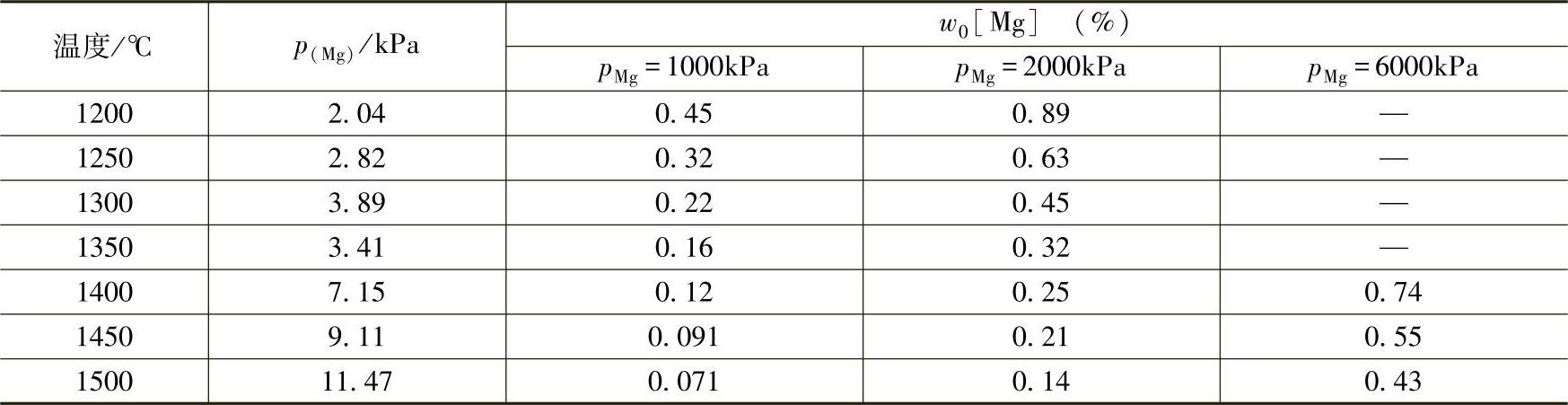
铁液中w0[Mg]、pMg、温度的关系见表2-14。
表2-14 铁液中镁的蒸气压和溶解度
③电石(CaC2)脱硫
2CaC2+5O2→2CaO+4CO2+20938kJ/kg
(CaO)+[FeS]→(CaS)+(FeO)
用于熔炼的电石中,CaC2的质量分数约为27%,为CaO-CaC2的共晶成分,熔点1670℃。
④金属氧化物脱硫。能脱硫的金属氧化物如CaO、MgO等均作为熔剂加入冲天炉内,进入渣中,经渣铁接触产生脱硫反应。由于这些氧化物在渣中的浓度已大为降低,且渣有较大黏度,从而使反应的动力学条件变差,达不到应有的脱硫效果。如果造成脱硫剂在炉内与铁液直接接触的条件,将克服上述的缺点,增大炉内脱硫的效果。将脱硫剂细小颗粒(50~100目)加入送风中,吹入炉内,就是出于此目的的一种有效方法。该方法的优点一是高度分散的脱硫剂细小颗粒直接与铁液滴及流股大面积接触,未经造渣,保持了本身的氧化物含量;二是铁液滴流过程中,不断有脱硫剂附着,形成有利的表面扩散条件;三是脱硫剂与铁液接触的区域是风口区,温度高。
2)炉外脱硫。炉外脱硫的办法是向铁液中加入脱硫剂,并通过搅拌促进脱硫剂在铁液中的扩散,以加快脱硫反应并充分利用脱硫剂。
①合金元素的脱硫作用。利用与硫亲和力大于Fe的合金元素,在铁液中置换FeS中Fe,形成新的高熔点的或不溶于铁液的硫化物,把硫从铁液中脱除。
常用的脱硫剂如Ce、Ca、Na、Mg、Mn等金属以及它们的合金。按与硫亲和力从大到小可排成如下顺序:Ce>Ca>Mg>Na>Mn>Fe。以Mi代表各金属,脱硫反应的通式可表为
[FeS]+[Mi]→(MiS)+[Fe]
②碱金属、碱土金属化合物的脱硫作用
CaO、Na2CO3、BaO等具有脱硫作用。例如用碳酸钠脱硫时,发生下列反应
Na2CO3→Na2O+CO2-Q
[FeS]+(Na2O)→(Na2S)+[FeO]
而产生的[FeO]又被铁液中的C、Si、Mn还原而去除。
Na2CO3脱硫过程中产生大量气体,对铁液和渣剧烈搅拌,促进脱硫反应进行。
碳酸钠的脱硫反应可简化为Na2O+[S]+[C]→Na2S+CO
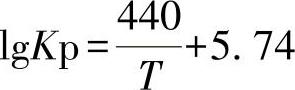
Na2CO3脱硫时,如果渣中存在较多的SiO2,可能发生回硫反应
(Na2S)+(SiO2)+(FeO)→(Na2SiO3)+[FeS]
氧化钙的脱硫反应可简化为
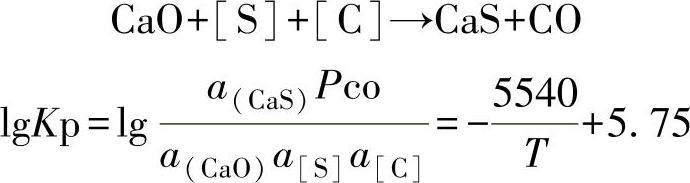
热力学分析表明,这些化合物作为脱硫剂都有较强的脱硫作用。
炉外脱硫的过程中,铁液温度都会下降,如果温度过低,不但使脱硫率降低,而且由于低温铁液黏度增大,使反应生成的杂质不易上浮,可能造成铸件夹杂。所以不论用什么方法进行炉外脱硫,铁液的出炉温度至少不应低于1450℃;而对于质量要求较高的铸件,铁液出炉温度应超过1500℃。
4.铁液含磷量的变化
(1)冲天炉铁液中的磷含量 除用于耐磨铸件的含磷耐磨铸铁外,磷在铸铁中是有害杂质。
根据我国的资源情况和生产条件,冲天炉熔炼的铁液中,通常含磷量在0.1%~0.12%。对于力学性能要求不高的铸铁尚可允许,但对要求高的铸件,磷含量应小于0.08%,甚至更低。
(2)降低铁液中磷含量的方法 在冲天炉环境中,溶于铁液中的磷,与硅、锰、碳、铁元素共存,如图2-39所示,高于900℃时,磷与氧的亲和力低于硅、锰、碳、铁。从热力学条件看,磷在铁液中氧化烧损是困难的,而且磷在铁液中的含量远低于上述其他元素,也不利于磷氧化反应的进行,尤其在酸性冲天炉内,由于P2O5为酸性氧化物,易被上述元素还原而重新溶入铁液中,使得炉料及铁液中的磷基本上没有因为氧化烧损而减少。因此,在冲天炉熔炼中,铁液含磷量被认为是不变的,这也由生产实践所证明。
铁液脱磷的反应为:2[P]+5(FeO)+(CaO)→(CaO·P2O5)+5[Fe]+Q
脱磷反应过程是铁液中的P先被渣中FeO氧化成P2O5,进入渣中的P2O5再与渣中的CaO结合成稳定的复合氧化物CaO·P2O5。反应难于进行的原因是:
①磷与氧的亲和力在900℃以下才高于Fe,所以FeO被P还原的反应需要低温条件。在冲天炉条件下,反应只能在料块表面进行,动力学条件很差。
②在低温条件下,炉渣中CaO和FeO的浓度要足够高,才能弥补低温条件下反应动力学条件的不足。因此,需要造高碱度的氧化渣,这在碱性冲天炉中是可行的,而在酸性冲天炉内是不可行的。炉内脱硫的条件是高温,渣中FeO浓度低,正与脱磷的条件相反。所以即使在碱性炉的熔炼环境中,也难于实现同时脱硫和脱磷。这是冲天炉熔炼中不采取脱磷措施的原因。由于铁液中的含磷量在冲天炉熔炼中基本不变,所以,一般是通过控制炉料的含磷量来控制铁液的含磷量。
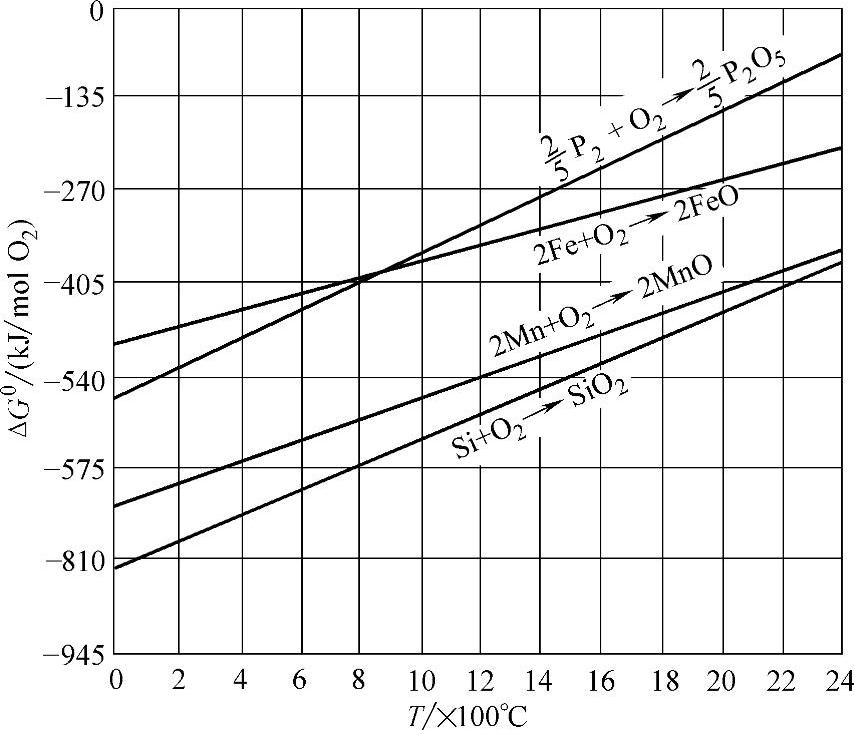
图2-39 P、Fe、Mn、Si的氧化物生成自由能
相关文章

本节以最为常用的电磁感应水冷铜坩埚凝壳熔炼为例,介绍钛合金熔炼时的基本特征。由图可知,开始保温之后,随着保温时间的延长,凝壳质量分数fskull急剧减小,这是因为输入的能量大于熔体通过冷坩埚和热辐射损失的能量,使得之......
2025-09-29

2.除锈铁锈的主要成分是FeO、Fe2O3、Fe3O4等,“四合一”处理液含有较高浓度的磷酸,其总酸度和游离酸度比普通磷化液要高得多,这些铁锈在游离酸的作用下被除去,反应式为FeO+2H3PO4→Fe2+H2O (5-9)Fe2O3+6H3PO4→2Fe3+3H2O Fe3O4+8H3PO4→Fe2+2Fe 3+4H2O 由于除锈能力强的盐酸和硫酸不能成膜,还会对磷酸盐膜产生破坏作用,所以处理液中不含盐酸和硫酸,只含磷酸,而磷酸除锈能力不太强,对于重锈所需的除锈时间太长,不利于后续处理。......
2025-09-29

打浆过程中纤维的变化,主要可分为5个方面:细胞壁的位移和变形,初生壁和次生壁外层的破除,润胀,细纤维化和切断等。因此,在打浆过程过程中,除了要将初生壁除去之外,还要把部分或全部次生壁外层除去,以利于纤维的润胀和细纤维化。纤维在极性液体中极易发生润胀。外部细纤维化是指在打浆过程中纤维受到打浆设备的机械作用而产生纵向分裂,并分离出细纤维,而且使纤维产生起毛和两端帚化的现象。......
2025-09-29

在讨论短路全电流表达式之前,应该首先了解短路电流各分量在暂态过程中的变化规律,即了解各自由电流衰减的时间常数。在暂态阶段中阻尼绕组的作用基本消失,被看做定子漏磁链的那部分电枢反应磁链Ψ″ad穿过阻尼绕组。在暂态阶段中只有暂态分量的衰减,而次暂态分量近似认为已衰减到零,这种情况相当于无阻尼绕组的同步发电机。......
2025-09-29

受制于气流扩散速度的燃烧称为扩散燃烧。图2-2 CO系各反应的ΔG0及KP随温度的变化在还原带,高于705℃,反应即可进行,而低于705℃时,CO2不能还原。碳的燃烧产物主要是CO2,当逐渐到达氧化带上部,氧气浓度下降,C、O2分子碰撞的次数大幅减少时,CO才能逐渐增多。假设O2、CO2、CO等气体的体积分数仅沿底焦的高度变化,且在底焦横截面上均匀分布。......
2025-09-29

发动机冷却液由水、防冻剂和各种添加剂组成。1)缓蚀剂缓蚀剂是冷却液中最主要的添加剂,其主要作用是减缓或防止冷却系统中金属零部件因腐蚀而穿孔,以免造成冷却液渗漏和流失。3)防垢剂为了防止冷却系统内水垢的产生,有的冷却液中还含有一定量的防垢剂。......
2025-09-29

在合金的真空熔炼过程中,元素的挥发损失将主要是Al元素的挥发损失。真空熔炼的目的是避免气氛中间隙元素对合金的污染,而TiAl合金熔体中的主要成分铝具有较高的饱和蒸气压,在真空熔炼过程中极易产生挥发损失,严重影响合金成分的准确性,而且挥发产物污染真空系统。因此熔炼TiAl合金时,为了防止合金熔体中铝的沸腾,真空度不宜过高,应不超过临界值。......
2025-09-29
相关推荐