【摘要】:图4-3电化学腐蚀与阴极保护a)自然腐蚀b)牺牲阳极阴极保护c)外加电流阴极保护外部阴极极化电流的提供有两种方式,对应于两种阴极保护方法,如图4-3所示。宏观腐蚀电池的阳极由于发生金属的溶解反应而不断被消耗掉,因此采用这种方式的阴极保护称为牺牲阳极法阴极保护。
根据金属电化学腐蚀的原理,发生金属电化学腐蚀必然是因为在金属表面存在着电位不相等的区域。金属的电化学腐蚀可以用图4-1a所示的模型来说明。
金属发生电化学腐蚀的根本原因在于金属表面存在电位不同的区域,且组成了一个腐蚀原电池。腐蚀原电池是短路了的原电池,如图4-1a所示。对于一个完全纯净的金属而言,表面不存在电位不同的区域,整个表面都应该是该金属在腐蚀介质中的平衡电极电位。但实际上,金属中总是掺有各种杂质或者存在晶格缺陷,这些区域的电极电位要高于金属本身的电极电位。金属相电位极低,成为原电池的阳极,它的平衡电极电位用φa表示;杂质相或晶格缺陷的区域电极电位较高,成为原电池的阴极,它的起始平衡电极电位用φc表示,如图4-2所示。
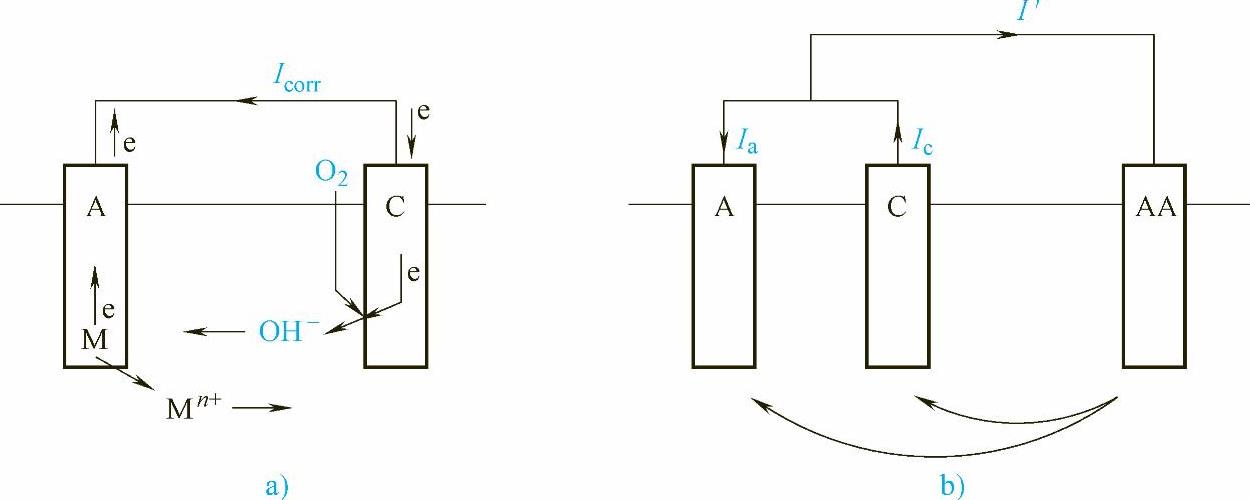
图4-1 阴极保护模型
a)腐蚀原电池 b)阴极保护原理
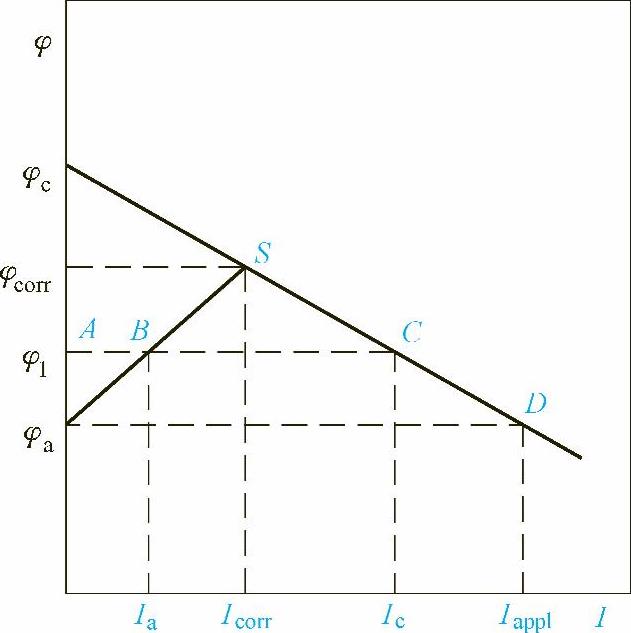
图4-2 阴极保护原理的极化图
当该金属处于腐蚀介质中时,腐蚀原电池中就会有电流产生,阳极发生金属的溶解反应:
M→Mn++ne
阴极主要发生去极化剂的阴极还原反应,在大多数情况下,阴极去极化剂是空气中的氧,所以阴极主要发生氧的阴极还原反应:
O2+2H2O+4e→4OH-(碱性条件下)
O2+4H++4e→2H2O(中性或弱酸性条件下)
这样阳极与阴极都在腐蚀电流的作用下发生极化,阳极极化的结果是阳极电极电位正移,阴极极化的结果是阴极的电极电位负移,如图4-2所示。随着腐蚀电流的增大,阳极电位不断正移,阴极电位不断负移,当两者相等时(即图4-2上的S点),整个金属表面形成一个等电体,就不会再发生电位移动了。这时金属表面就形成一个稳定电位,我们称为腐蚀电位或自然电位φcorr。这个电位是在电流的极化下才能达到的,所以为了维持这个腐蚀电位所需的电流就称为腐蚀电流Icorr。这是在自然状态下,金属达到稳定状态时的腐蚀电流,表示了金属的腐蚀速度。
从本质上讲,金属腐蚀的速度是受Ia控制的,但在自然腐蚀状态下,Ia=Ic=Icorr,如果再引入一个辅助阳极AA,通过AA向金属引入一个外部阴极极化电流,如图4-1b所示,情况就会发生变化。由于外部电流的极化,使金属表面的电位能够进一步负移。在图4-2中的阴极极化曲线φcS从S点向C点方向延长。
当金属电位极化在外部电流的极化下负移到φ1时,在此电位下阴极的极化电流为Ic,阳极的极化电流为Ia,I′=Ic-Ia就是外加的极化电流。从图4-2中可以看出,Ia比Icorr小得多,说明在外加阴极极化电流的情况下,金属的腐蚀速度有所减缓,但还没有完全停止腐蚀。
如果进一步加大外部阴极极化电流,使金属的阴极极化进一步负移到φa处,这时由于极化使金属表面各个区域的电位都等于φa,即金属的平衡电极电位。当金属处于平衡电极电位时,电极的净反应速度为零,即金属的腐蚀电流为零,金属不再发生溶解反应,因而得到了完全的保护。这时外加的电流Iappl即为达到完全保护所需的最小电流。如果再加大外部极化电流,金属的电位还将负移,此时金属表面原来的阳极区域也将发生氧的还原反应,提供阴极电流,从而使阳极区的电流方向发生改变。

图4-3 电化学腐蚀与阴极保护
a)自然腐蚀 b)牺牲阳极阴极保护 c)外加电流阴极保护
外部阴极极化电流的提供有两种方式,对应于两种阴极保护方法,如图4-3所示。一种是在腐蚀体系中引入一个电极电位更负的金属或合金电极,与被保护金属电连接成一个宏观腐蚀电池,由于两者之间的电位差,形成一个宏观腐蚀电流流入被保护金属,使其电极电位负移。宏观腐蚀电池的阳极由于发生金属的溶解反应而不断被消耗掉,因此采用这种方式的阴极保护称为牺牲阳极法阴极保护。极化电流的大小取决于宏观腐蚀电池之间的电位差以及腐蚀介质的电导率。采用牺牲阳极法阴极保护就需要选用电极电位较负的金属或合金,同时必须保证腐蚀介质有足够的电导率,所以该法主要用于海水、土壤中金属的防腐处理。
另一种方法是在腐蚀体系中引入一个惰性阳极,同时通过外部直流电源提供一个极化电流,使被保护金属处于阴极极化中,这种方法称为外加电流法阴极保护。它的显著优点是应用范围广,可以通过调节外加电流的大小使金属得到完全的保护。此方法的缺点是必须要有外部的直流电源,所以一些野外无电源的地区无法应用。
这两种阴极保护方法都会在以下小节中进行详细的说明。











相关推荐