集油管一般用直径为200~300mm的钢管制成,沿其长度在管壁的一侧开有切口,集油管可以绕轴线转动。图2-22平流隔油池刮油刮泥机由钢丝绳或链条牵引,移动速度不大于2m/min。在寒冷地区集油管及油层内宜设加热设施。隔油池每个格间的宽度,由干刮泥刮油机跨度规格的限制,一般为2.0m、2.5m、3.0m、4.5m和6m。采用人工清除浮油时,每个格间的宽度不宜超过6.0m。有效水深一般为1.5~2.0m。其构造如图2-23所示。......
2023-06-19
铁和锰的化学性质相近,所以常共存于地下水中,但铁的氧化还原电位低于锰,容易被O2氧化,相同pH时二价铁比二价锰的氧化速率快,以致影响二价锰的氧化,因此地下水除锰比除铁困难。
地下水中Mn2+被O2氧化时的动力学和铁的氧化不同,[Mn2+]随时间t的变化不再是线性关系,而且在pH<9.5时,Mn2+的氧化速率很慢。试验结果认为,Mn2+的氧化和去除是自动催化氧化过程,反应如下:

式中:[Mn2+]0——开始时二价锰浓度,mol/L;
[Mn2+]——时间,时的二价锰浓度,mol/L;
K——自动催化反应速率常数;
A——常数。
锰的氧化速率也和[OH-]2以及PO2成正比,但是在更高pH时才可使氧化较快,也就是pH值高时除锰较易。
除锰时的自动催化性质表现在:在反应过程中缓慢生成MnO2沉淀,然后水中Mn2+离子很快吸附在MnO2上成为Mn2+MnO2,此后吸附的Mn2+离子以缓慢的速度氧化。
除锰时所采用的工艺流程为:
![]()
上述工艺适用于含铁量小于2.0mg/L、含锰量小于1.5mg/L时。
曝气装置和除铁时相同,根据锰氧化时的反应:
![]()
从化学计量关系,每氧化lmg/LMn2+需氧![]() mg/L,同时产生0.036mg/LH+。实际上所需氧量较理论值为高。
mg/L,同时产生0.036mg/LH+。实际上所需氧量较理论值为高。
过滤可以采用各种形式滤池。在同一滤层中,铁主要截留在上层滤料内。当地下水中铁锰含量不高时,可上层除铁下层除锰而在同一滤层中去除,不致因锰的泄漏而影响水质。但如含铁、锰量大,则除铁层的范围增大,剩余的滤层不能截留水中的锰,因而部分泄漏,滤后水不符合水质标准。显然,原水含铁量越高,锰的泄漏时间将越早,因此缩短了过滤周期,所以铁对除锰的干扰是除铁除锰时须注意的问题。这时为了防止锰的泄漏,可在流程中建造两个滤池,前面是除铁滤池,后面是除锰滤池。在压力滤池中也有将滤层做成两层,上层用以除铁,下层用以除锰,如图2-7所示。
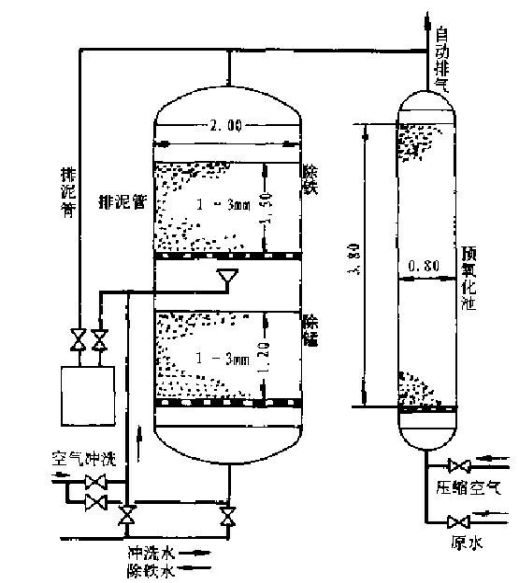
图2-7 除铁除锰双层滤池
除锰滤池的滤料可用石英砂或锰砂,滤料粒径、滤层厚度和除铁时相同。滤速为5~8m/h,石英砂滤料的冲洗强度为12~14L/s·m2,膨胀率为28%~35%,冲洗时间5~15min。
除锰滤池成熟后,滤料上有催化活性的滤膜,外观为黑褐色,据仪器分析,它的成份是高价铁锰混合氧化物,以铁锰为主,可优先吸附Mn2+、Fe2+、Ca2+等并进行催化氧化反应而沉积在滤料上,使活性滤膜不断增长。它是使Mn2+较快地形成高锰氧化物的催化剂,并且是在除铁除锰很短的曝气、过滤过程中,能够氧化和去除Mn2+的原团。
除锰过程中,除了溶解氧将水中Mn2+氧化成MnO2,再加某些催化剂参与反应外,也不能忽视铁细菌的作用。微生物的生化反应速率远大于溶解氧氧化Mn2+的速率,随着滤料的成熟,可观测到滤料上或滤料孔隙之间有铁细菌群体,数量约为10~20×104个/mL,对于长成活性滤膜有促进作用。
有关工业水处理技术的文章

集油管一般用直径为200~300mm的钢管制成,沿其长度在管壁的一侧开有切口,集油管可以绕轴线转动。图2-22平流隔油池刮油刮泥机由钢丝绳或链条牵引,移动速度不大于2m/min。在寒冷地区集油管及油层内宜设加热设施。隔油池每个格间的宽度,由干刮泥刮油机跨度规格的限制,一般为2.0m、2.5m、3.0m、4.5m和6m。采用人工清除浮油时,每个格间的宽度不宜超过6.0m。有效水深一般为1.5~2.0m。其构造如图2-23所示。......
2023-06-19

流网由一组流线和一组等势线组成。如图1-8所示的一维流动情况,实际上没有必要绘制流网,直接应用达西定律就可计算流量、确定各点的水头和水头差。基坑中段可看作是二维稳定渗流问题,此时要计算渗流量以及土层中各点的水头损失,只有靠绘制流网最为方便。图1-23流网绘制(图试法)判定边界条件,如a′a和bb′为等势线(透水面);acb和OO′为流线。......
2023-09-23

使用node.replaceChild将旧的子节点oldChildNode替换为新的子节点newChildNode,并返回被替换的子节点,语法如下:参数说明:◇ parentNode:表示父节点。◇ oldChildNode:必选参数,表示要被替换的子节点。oldChildNode必须是parentNode的直接子节点。动手写14.4.12执行14.4.12.html,输出结果到网页,如下图所示。图14.4.12使用node.replaceChild替换节点提示使用newChildNode替换oldChildNode时,如果newChildNode已经存在于DOM树结构中,则newChildNode会先从原始位置移除。......
2023-11-08

含铁地下水由于在地下,铁是以Fe2+状态存在。这个过程称为曝气除铁,其反应如下曝气后的水再经过滤处理即可除去Fe3沉淀物。跌水高度一般在0.5~1.0m时,即可满足含铁量在5~10mg/L的地下水除铁的要求。在低pH值下,不利于除铁反应的进行。图2-5加气阀曝气除铁系统1—水泵;2—吸水管;3—加气阀;4—空气混合水;5—除铁水;6—锰砂过滤器;7—清水图2-6加气阀结构图锰砂除铁一般适合于地下水含铁量小于20mg/L的除铁。......
2023-06-19

◇ tagName:必选参数,标签名称。动手写14.4.3执行14.4.3.html,输出结果到网页,如下图所示。图14.4.3使用document.createElement创建元素DOM支持创建任意名称的标签,和普通标签一样可以正常使用。图14.4.4使用浏览器解析HTML字符串创建元素使用浏览器解析HTML可以方便地创建DOM树形结构,实际应用中时常采用拼接HTML字符串来实现局部修改。......
2023-11-08

异养菌分为本身能从水质中摄取无机物或有机物而生活的腐生菌和依赖寄主供给营养的寄生菌两类。通常所说的异养菌指的是存在于水中的腐生菌。在循环冷却水中,异养菌不仅生长繁殖快,而且为数多,基本上代表了水中全部好氧菌的数量,所以一般在测定时,以这类细菌的数量作为细菌总数。循环冷却水中异养菌数的监测频率应为1次/周。对菌落计数用平皿计数法对异养菌的菌落进行计数,然后再计算每毫升水样中的异养菌数。......
2023-06-30

传统文化元素悠久的历史,别具一格的风范与多样的形态,为人类历史谱写了充满智慧与灵性之光的篇章,具象化的传统文化元素是中国古代劳动人民为满足自身需要创造出的智慧的结晶。将传统文化元素的形态运用于当代艺术设计中,使得设计作品增添了古色古香的中国韵味,同时为消费者带来了一份文化归属感,能在一定程度上与消费者内心产生共鸣,满足消费者的文化诉求。......
2023-06-23

未来气候变化极有可能对山东省未来水资源分布产生更为显著的影响,对山东省南水北调水资源配置工程、江河防洪体系规划和流域生态环境修复与建设等重大工程的预期效果产生不利影响。由于气候变化影响的山东省区域特性,当前迫切需要开展气候变化对山东省水安全影响与适应性对策的基础研究,它是保障山东省水安全的重大战略需求,也是水科学前沿和应用基础问题。......
2023-06-25
相关推荐